
| A. | 中和10 mL 0.1 mol•L-1 醋酸与中和100 mL 0.01 mol•L-1的醋酸所需同种碱溶液的量不同 | |
| B. | 常温下,pH=3的甲酸溶液的c(H+)与pH=11的氨水溶液中,由水电离产生的c(OH-)相等 | |
| C. | 向NH4Cl溶液中逐渐加入适量NaOH固体,溶液的导电性明显增强 | |
| D. | 向饱和石灰水中加入少量CaO,恢复至室温后溶液中c(OH-)增大,导电能力增强 |
分析 A、10 mL 0.1 mol•L-1 醋酸与100 mL 0.01 mol•L-1的醋酸含有的CH3COOH物质的量相等,且两者均为一元酸;
B、甲酸、氨水均抑制水的电离;
C、溶液的导电能力取决于离子浓度大小;
D、温度不大,氢氧化钙的溶解度不变,则溶液的浓度不变,所得的仍为饱和溶液.
解答 解:A、10 mL 0.1 mol•L-1 醋酸与100 mL 0.01 mol•L-1的醋酸含有的CH3COOH物质的量相等,所以中和时所需同种碱溶液的量相等,故A错误;
B、甲酸、氨水抑制水的电离,则常温下,pH=3的甲酸溶液的c(H+)与pH=11的氨水溶液中,由水电离产生的c(OH-)相等,故B正确;
C、向NH4Cl溶液中逐渐加入适量NaOH固体生成氯化钠和一水合氨,溶液的导电性无明显变化,故C错误;
D、向饱和石灰水中加入少量CaO,恢复至室温后溶液仍然是饱和溶液,c(OH-)不变,导电能力不变,故D错误.
故选B.
点评 本题考查了酸碱混合溶液定性判断及溶液pH的计算,题目难度中等,根据酸碱的相对强弱再结合物质的性质分析解答,注意A中消耗碱的物质的量与酸的浓度无关,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 第一电离能由小到大的顺序是S<P<Cl | |
| C. | 47Ag原子的价层电子排布式是4d95s2 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是p区元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/LNaCl溶液 | B. | 2mol/LNH4Cl溶液 | ||
| C. | 1.5mol/LMgCl2溶液 | D. | 2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 温度一定,一个化学反应的平衡常数是一个常数 | |
| B. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| C. | 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 | |
| D. | 浓度商Qc<Kc,v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥⑤④⑧⑦⑨ | B. | ①②⑤③⑥④⑧⑦⑨ | C. | ①②③④⑤⑧⑥⑦⑨ | D. | ①②③⑤⑥④⑧⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCH2Cl2含有分子的数目为0.1NA | |
| B. | 电解精炼铜时,阳极质量减少12.8g时,转移电子0.4NA | |
| C. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| D. | 常温常压下,将0.1mol Fe投入足量的稀硝酸中,转移的电子为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
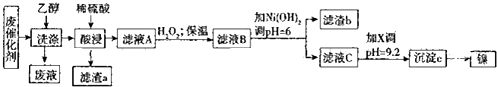
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L的盐酸溶液和0.1 mol/L的NaOH溶液 | |
| B. | pH=1的盐酸溶液和pH=13的Ba(OH)2溶液 | |
| C. | pH=4的醋酸溶液和pH=10的NaOH溶液 | |
| D. | pH=4的盐酸溶液和pH=10的NH3•H2O溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com