
| A、①②⑤ | B、①②④ |
| C、②④⑤ | D、全部 |


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
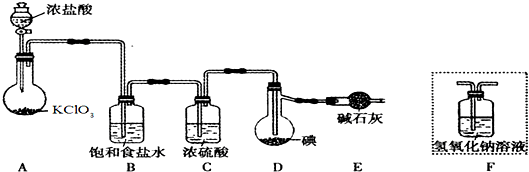

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤④② |
| B、③⑤①④② |
| C、③⑤①⑥② |
| D、③⑤①⑥④② |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
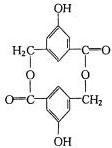 A、B、C、D均为含有苯环的有机物,且式量B>A>C.己知有机物A既能和氢氧化钠溶液反应,又能和 NaHCO3溶液反应,并已知A的化学式为C7H6O3,且它的苯环上一氯代物有两种.
A、B、C、D均为含有苯环的有机物,且式量B>A>C.己知有机物A既能和氢氧化钠溶液反应,又能和 NaHCO3溶液反应,并已知A的化学式为C7H6O3,且它的苯环上一氯代物有两种.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.06 g |
| B、3.1 g |
| C、5.3 g |
| D、9.0 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com