
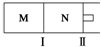
 M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.隔板Ⅰ固定不动,活塞Ⅱ可自由移动.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.隔板Ⅰ固定不动,活塞Ⅱ可自由移动.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A. | 若x:y=1:2,则平衡时,M中的转化率:A>B | |
| B. | 若x:y=1:3,当M中放出热量172.8 kJ时,A的转化率为90% | |
| C. | 若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.4mol A时,v正>v逆 | |
| D. | 起始时,分别向M、N两个容器中加入1molA和1molC,达到平衡时,容器M、N中物质A的体积分数:M<N |
分析 M容器保持恒容,N容器保持恒压,由于反应前后的气体系数和不等,所以两个平衡态也不一样,
A、由于x:y=1:2,即y=2 x,设反应中消耗掉amolA,用a表示参加反应的B的物质的量,表示出转化率,据此比较;
B、题目中热化学方程式的意义为1molA完全反应,放热192 kJ,根据实际放出的热量计算参加反应的A的物质的量,进而表示出转化率进行判断;
C、根据平衡时C的物质的量,利用三段式计算出平衡时各组分的物质的量,进而计算平衡常数.再通入0.4 molA时,假定平衡不移动,恒温恒压下,体积之比等于物质的量之比,据此计算通入0.4 molA时瞬间体积,再计算各物质的量的浓度,进而计算浓度商,与平衡常数比较,判断平衡移动,据此确定;
D、加入1molA、1molC相当于加入1.5molA、1.5molC,由于压强不同,达到平衡时A的体积分数不同.
解答 解:M容器保持恒容,N容器保持恒压,由于反应前后的气体系数和不等,所以两个平衡态也不一样,
A、x:y=1:2,即y=2 x,设反应中消耗掉amolA,则:
A(g)+3B(g)?2C(g)
初始(mol):x 2x 0
变化(mol):a 3a 2a
故A的转化率=$\frac{a}{x}$,B的转化率=$\frac{3a}{2x}$,则平衡时,M中的转化率:A<B,故A错误;
B、题目中热化学方程式的意义:若1molA完全反应,放热192 kJ,当M中放出热量172.8 kJ时,参加反应的A的物质的量为$\frac{172.8kJ}{192kJ}$×1mol=0.9mol,故A的转化率为$\frac{0.9}{x}$,故B错误;
C、x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,则:
A(g)+3B(g)?2C(g)
起始:1.2 1
反应:0.2 0.6 0.4
平衡:1 0.4 0.4
故A、B、C的平衡浓度分别为0.5mol/L、0.2mol/L、0.2mol/L,
则平衡常数K=$\frac{0.{2}^{2}}{0.5×0.{2}^{3}}$=10
原平衡体系中,2.0L容器中含有分子物质的量为1.0+0.4+0.4mol=1.8mol,当加入0.4molA,体系瞬间有分子物质的量为(1.8+0.4)mol=2.2mol,N容器恒温、恒压,则容器体积比=气体的物质的量比,即:2.2mol:1.8mol=V:2L,瞬间总体积(V)变为$\frac{2.2mol×2L}{1.8mol}$=2.44L,此时的浓度商Qc=$\frac{(\frac{0.4}{2.44})^{2}}{\frac{1.4}{2.44}×(\frac{0.4}{2.44})^{3}}$=10.6,Qc>K,所以,平衡要逆向移动,即v(正)<v(逆),故C正确;
D、起始时,分别向M、N两个容器中加入1molA、1molC,相当于加入1.5molA、1.5molC;由于M和N的反应条件不同,该反应又是体积缩小的反应,N中压强大于M,平衡向着正向移动,所以达平衡时,容器M中物质A的体积分数大于N,故D错误;
故选C.
点评 本题考查化学平衡的计算、平衡常数的计算等,难度较大,D选项为易错点、难点,注意根据平衡常数判断平衡移动方向,A选项中注意数据的分析处理.


科目:高中化学 来源: 题型:多选题
| A. | 甲苯分子中所有原子可能共平面 | |
| B. | 只有水就能区别苯、酒精、四氯化碳这三种无色液体 | |
| C. | 在化学反应过程中,发生物质变化的同时一定发生能量变化 | |
| D. | 埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更难被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可使蛋白质变性,故可浸制标本 | |
| B. | 海水提取溴、煤的液化、纯碱去油污都发生了化学变化 | |
| C. | 钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高 | |
| D. | Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、乙烯、苯都可通过石油分馏得到 | |
| B. | 乙醇既能与有机化合物反应又能与无机化合物反应 | |
| C. | 煤焦油、石油、花生油都属于烃 | |
| D. | 鸡蛋清中加入饱和(NH4)2SO4溶液会使蛋白质失去生理活性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚类和醇类具有相同的官能团,因而具有相同的化学性质 | |
| B. | 含有羟基的化合物属于醇类 | |
| C. | 羟基跟链烃基直接相连的化合物属于醇类 | |
| D. | 分子内含有苯环和羟基的化合物都属于酚类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,若有6mol电子发生转移,则有2mol K2FeO4被氧化 | |
| B. | 放电时,正极反应为:FeO42-+4H2O+3e-═Fe(OH)3+5OH- | |
| C. | 充电时,电池的负极与外接电源的正极相连 | |
| D. | 充电时,阴极附近溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯和乙烯性质相似,都能发生加成反应 | |
| B. | 纤维素、橡胶和光导纤维都属于有机高分子化合物 | |
| C. | 乙烯和乙醇都可发生加成反应 | |
| D. | 等量的CH4和Cl2在光照下反应不能生成纯净的CH3Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 使用催化剂 | C. | 增大H2浓度 | D. | 减小压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com