
| A、Ag2S沉淀溶解平衡表达式:Ag2S?2Ag++S2- |
| B、硫代硫酸钠溶液和稀硫酸反应:SO42--+S2O32-+6H+=3SO2↑+3H2O |
| C、碳酸氢钠溶液与足量的氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D、酸性高锰酸钾与草酸反应:MnO4-+H2C2O4+2H+=MnO2+2CO2↑+2H2O |


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
 )的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色.K与过量NaOH溶液共热,发生反应的方程式为
)的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色.K与过量NaOH溶液共热,发生反应的方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①③④ |
| C、①②③ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | ||||
| B、向10mL 1.5mol?L-1NaHSO4溶液中加入10mL 1mol?L-1Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O | ||||
| C、工业用石灰乳制漂白粉:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O | ||||
D、向20mL沸水中滴入1mL饱和FeCl3溶液,继续煮沸至溶液呈红褐色:Fe3++3H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol 硫酸钾中阴离子所带电荷数为NA |
| B、乙烯和环丙烷(C3H6)组成的28g混合气体中含有NA个氢原子 |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠溶液吸收过量的二氧化碳 OH-+CO2=HCO3- |
| B、亚硫酸氢铵溶液与足量氢氧化钠溶液反应 HSO3-+OH-=SO32-+H2O |
| C、氯气通入冷水中 Cl2+H2O=Cl-+ClO-+2H+ |
| D、碳酸镁悬浊液中加醋酸 CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | ||||||||||
| B、向Cr2O72-+H2O?2CrO42-+2H+的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色 | ||||||||||
C、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)
| ||||||||||
D、已知:
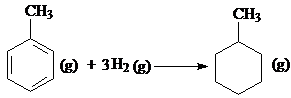 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| HCl |
| 水解 |
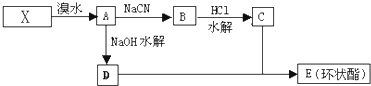
查看答案和解析>>
科目:高中化学 来源: 题型:
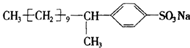 ,其结构中与肥皂(C17H35COONa)的憎水基团-C17H35相当的基团为
,其结构中与肥皂(C17H35COONa)的憎水基团-C17H35相当的基团为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com