
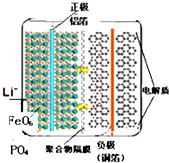
| A. | 放电时,铝箔所在电极为负极,铜箔所在电极为正极 | |
| B. | 放电时,电池反应式为:FePO4+Li═LiFePO4 | |
| C. | 充电时,Li+向阴极移动 | |
| D. | 充电时,阳极的电极反应式为:LiFePO4-e-═FePO4+Li+ |
分析 充电时,LiFePO4中的锂离子脱出并伴随着铁元素的氧化,则铝电极失电子发生氧化反应,为阳极,铜电极为阴极,阴极上锂离子得电子发生还原反应,所以阳极反应式为LiFePO4-e-═FePO4+Li+、阴极反应式为Li++e-=Li;放电时,正极、负极反应式正好与阳极、阴极反应式相反,据此分析解答.
解答 解:充电时,LiFePO4中的锂离子脱出并伴随着铁元素的氧化,则铝电极失电子发生氧化反应,为阳极,铜电极为阴极,阴极上锂离子得电子发生还原反应,所以阳极反应式为LiFePO4-e-═FePO4+Li+、阴极反应式为Li++e-=Li,放电时,正极、负极反应式正好与阳极、阴极反应式相反,
A.充电时铝电极为阳极、铜电极为阴极,则放电时,铝电极为正极、铜电极为负极,故A错误;
B.放电时,负极上锂失电子发生氧化反应、正极上磷酸铁得电子发生还原反应,所以电池反应式为FePO4+Li═LiFePO4,故B正确;
C.充电时,阳离子向阴极移动,所以Li+向阴极移动,故C正确;
D.充电时,阳极上失电子发生氧化反应,所以阳极的电极反应式为:LiFePO4-e-═FePO4+Li+,故D正确;
故选A.
点评 本题考查化学电源新型电池,为高考高频点,正确理解“充电时,LiFePO4中的锂离子脱出并伴随着铁元素的氧化”是解本题关键,难点是电极反应式的书写,知道离子移动方向,题目难度不大.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH5的熔沸点低于N3的熔沸点 | |
| B. | NH5中N元素显+5价 | |
| C. | NH5固体投人稀盐酸中,会生成氨气和氩气 | |
| D. | NH5中滴人少量的水时会剧烈反应,该反应的化学方程式可表示为山NH5═NH3↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 当v逆(X)=2v正(Z),可以说明反应达平衡 | |
| B. | 反应前2 min的平均速率v(Z)=4.0×10?3 mol•L?1•min?1 | |
| C. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 | |
| D. | 该反应在350℃时的平衡常数小于1.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质氧化性F2>Cl2>Br2>I2,因此排在前面的卤素单质均可将排在后面的卤素从它的盐溶液中置换出来 | |
| B. | 卤族元素从C1到I,最高价氧化物对应水化物的酸性减弱 | |
| C. | 卤族元素从F到I,HX水溶液酸性增强 | |
| D. | 卤素单质从F2到I2颜色加深,熔沸点升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
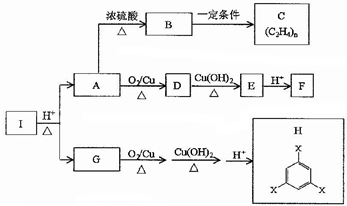
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;反应类型:取代反应
;反应类型:取代反应 ;反应类型:加聚反应
;反应类型:加聚反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤ | C. | ①②⑥ | D. | ③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白磷(P4)易溶于CS2,但难溶于水 | B. | NaCl易溶于水,难溶于CCl4 | ||
| C. | 碘易溶于苯,微溶于水 | D. | 卤化氢易溶于水,也易溶于CCl4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com