
(2004·黄冈)如下图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题.

(1)实验中观察到的现象是_______________________________________.
(2)产生上述现象的原因是_______________________________________.
(3)写出有关反应的离子方程式___________________________________
_____________________________________________________________.
(4)由实验推知,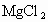 溶液和
溶液和 的总能量________(填“大于”“小于”“等于”)镁片和盐酸的总能量.
的总能量________(填“大于”“小于”“等于”)镁片和盐酸的总能量.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:022
(2004·黄冈)近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展,像电一样,氢是一种需要依靠其他能源如石油、煤、原子能等的能量来制取的所谓“二级能源”,而存在于自然界的可以提供现成形式能量的能源称为一级能源,如煤、石油、太阳能和原子能等.
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是
[ ]
(2)氢气燃烧时耗氧量小,发热量大.已知热化学方程式为


试通过计算说明等质量的氢气和碳燃烧时产生热量的比是___________.
(3)氢能源有可能实现能源的贮存,也有可能实现经济、高效的输送.研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如: 、
、 、
、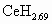 、
、 、
、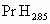 、
、 .已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为
.已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为 ,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式____________.
,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式____________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com