
����Ŀ���״���һ����Ҫ�Ļ���ԭ������һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ����
(1)��һ�ݻ�Ϊ2 L���ܱ������ڣ�����0.2 mol CO��0.4 mol H2������Ӧ��CO(g)+2H2(g)![]() CH3OH(g)��CO��ƽ��ת�������¶ȣ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)��CO��ƽ��ת�������¶ȣ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
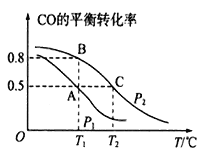
��A��B�����Ӧ��ѹǿ��С��ϵ��PA _______PB������>��<��=������
����ѹǿΪP2ʱB��C���������Ӧ���ʴ�С��ϵ��______________
������������˵��������Ӧ�Ѵﵽ��ѧƽ��״̬����__________
A��H2������������CH3OH�������ʵ�2�� B��CH3OH������������ٸı�
C�����������ܶȲ��ٸı� D��CO��CH3OH�����ʵ���֮�ȱ��ֲ���
(2)��ѹǿΪP1���¶�ΪT1 ��ʱ��H2��ƽ��ת����Ϊ__________(��������)���ټ���1.0 mol CO�����µ���ƽ�⣬��CO��ת����___________������������䡱��С������
(3) ��ѹǿΪP1���¶�ΪT1 ��ʱ��1L���ܱ������ڷ���������Ӧ�����ijʱ�̸����ʵ����ʵ������£�CO��0.05 mol��H2��0.1mol��CH3OH��0.05mol����ʱv(��)________v(��)���>������<����=������
���𰸡�< v��(C)>v��(B) BD 50% ��С =
��������
��1���ٷ�ӦCO(g)+2H2(g)![]() CH3OH(g)������Ӧ�������������ʵ�����С�ķ�Ӧ����ѹƽ�������ƶ�����Ӧ��ת��������
CH3OH(g)������Ӧ�������������ʵ�����С�ķ�Ӧ����ѹƽ�������ƶ�����Ӧ��ת��������
��ѹǿ��ͬʱ�������¶ȣ����������淴Ӧ���ʶ�����
�۴ﵽ��ѧƽ��ʱ�������淴Ӧ������ȣ����ò�ͬ�����ʵķ�Ӧ���ʱ�ʾƽ��״̬ʱ������������һ��һ�棬�ҵ���ϵ��֮������������ֵ�Ũ�ȡ��ٷֺ������ֲ��䣻���ݻ�ѧƽ����������ɴ���������һϵ�������������䣬�������DZ仯���������ˣ��ſ����ж�ƽ��״̬���ݴ˷�����
��2��P1ѹǿ��T1��Cʱ��CO��ת����Ϊ0.5������CO��ת��������������H2��ת���ʣ������������䣬����һ�ַ�Ӧ���Ũ�ȣ����������һ��Ӧ���ת���ʣ�������ת�����ǽ��͵ģ�
��3�������ʱŨ���̺�ƽ�ⳣ���Ƚ��ж�ƽ����еķ���
��1���ٷ�ӦCO(g)+2H2(g)![]() CH3OH(g)������Ӧ�������������ʵ�����С�ķ�Ӧ����ѹƽ�������ƶ�����Ӧ��ת����������PA < PB��
CH3OH(g)������Ӧ�������������ʵ�����С�ķ�Ӧ����ѹƽ�������ƶ�����Ӧ��ת����������PA < PB��
�ʴ�Ϊ��<��
��ѹǿ��ͬʱ�������¶ȣ������淴Ӧ���ʶ�������ѹǿΪP2ʱ��C���B���¶ȸߣ���C������Ӧ���ʽϴ�
�ʴ�Ϊ��v��(C)>v��(B)
�۴ﵽ��ѧƽ��ʱ�������淴Ӧ������ȣ����ò�ͬ�����ʵķ�Ӧ���ʱ�ʾƽ��״̬ʱ������������һ��һ�棬�ҵ���ϵ��֮������������ֵ�Ũ�ȡ��ٷֺ������ֲ��䣻���ݻ�ѧƽ����������ɴ���������һϵ�������������䣬�������DZ仯���������ˣ��ſ����ж�ƽ��״̬���ݴ˷�����
A. H2���������ʺ�CH3OH�������ʶ���ʾ����Ӧ���ʣ������ж�ƽ��״̬��A�����
B. CH3OH������������ٸı䣬���ж�ƽ��״̬��B����ȷ��
C. ��Ϊ�����ݻ����䣬���������غ㶨��֪�����������������䣬��˻��������ܶ�ʼ�ղ��䣬��˻��������ܶȲ��ٸı䣬�����ж�ƽ��״̬��C�����
D. ��Ϊ���ŷ�Ӧ�Ľ��У���ƽ��֮ǰ��CO���ʵ������ϼ��٣�CH3OH�����ʵ����������࣬���CO��CH3OH�����ʵ���֮��һֱ�������CO��CH3OH�����ʵ���֮�ȱ��ֲ��䣬���ж�ƽ��״̬��D����ȷ��
�ʴ�Ϊ��BD��
��2����ѹǿΪP1���¶�ΪT1 ��ʱ��CO��ת����Ϊ0.5����CO�ļ�����Ϊ0.2mol��0.5=0.1mol�����H2�ļ�����Ϊ0.2mol�����H2ƽ��ת����Ϊ![]() ���ټ���1.0 mol CO��ƽ��������Ӧ�����ƶ������´ﵽƽ�⣬������ת��������CO��ת���ʼ�С��
���ټ���1.0 mol CO��ƽ��������Ӧ�����ƶ������´ﵽƽ�⣬������ת��������CO��ת���ʼ�С��
�ʴ�Ϊ��50%����С��
��3��������֪��Ϣ����һ�ݻ�Ϊ2 L���ܱ������ڣ�����0.2 mol CO��0.4 mol H2������Ӧ����ѹǿΪP1���¶�ΪT1 ��ʱ������ƽ��ʱCOת����Ϊ0.5����˿��г�����ʽ������¶��µ�ƽ�ⳣ����
CO(g) + 2H2(g)![]() CH3OH(g)
CH3OH(g)
��Ӧǰ(mol/L) 0.1 0.2 0
ת��(mol/L) 0.050.1 0.05
ƽ��ʱ(mol/L) 0.050.1 0.05
��ѧƽ�ⳣ��![]() ��
��
�������䣬1L���ܱ������ڷ���������Ӧ�����ijʱ�̸����ʵ����ʵ������£�
CO:0.05mol��H2:0.1mol��CH3OH:0.05mol���ɼ���˿̵�Ũ����![]() =K����˷�Ӧ����ƽ��״̬��v(��)=v(��)��
=K����˷�Ӧ����ƽ��״̬��v(��)=v(��)��
�ʴ�Ϊ��=��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ˮ�д��ڶ��ַ��Ӻ����ӣ�����ʵ������ͽ���һ������ȷ����(����)
A. ������ˮʹ��õ���Ϊ��õ�壬˵����Cl2
B. ����ʯ����Һ����Һ��죬˵������Һһ������HClO
C. ��KHCO3����������Ƶ���ˮ�У������ݲ�����˵����HClO
D. ����������ˮ�������ݳ���������һ����O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�������ܱ������н��з�Ӧ��2SO2(g)��O2(g)![]() 2SO3(g)����H<0�����и�ͼ��ʾ��������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
2SO3(g)����H<0�����и�ͼ��ʾ��������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
A. ͼ ��ʾ�¶ȶ�ƽ���Ӱ�죬�Ҽ��¶Ƚϸ�
��ʾ�¶ȶ�ƽ���Ӱ�죬�Ҽ��¶Ƚϸ�
B. ͼ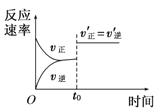 ��ʾt0ʱ�̺��ݳ���He(g)
��ʾt0ʱ�̺��ݳ���He(g)
C. ͼ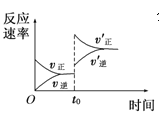 ��ʾt0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
��ʾt0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
D. ͼ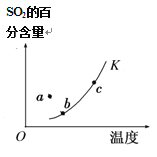 ��a��v�� > v��
��a��v�� > v��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.�����ϴ�������𣨼�ͭ�������ᣬ������������������˺Ͻ�Ӳ�ȷ��������
B.��ҵ����������ˮ��ʹ�õ��Ĺ�ͬԭ����![]()
C.̼������һ��ֱ��С��10nm�IJ��ϡ�������Ϊ��ɢ���γɵķ�ɢϵ��������
D.��Ȼ����һ�����Ļ�ʯȼ�ϣ���Ϊ����ԭ������Ҫ���ںϳɰ��ͼ״�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mLFeBr2��Һ��ͨ����������3.36L������ȫ������ԭ�������Һc(Br����=c(Cl������ԭ��Һ��FeBr2��Һ��Ũ��(mol��L��1)
A. 1 B. 1.5 C. 2 D. 2.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.�л���![]() ������Ϊ��2��3-����-7-���������
��������2��3-����-7-���������
B.1mol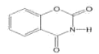 ������뺬3mol NaOH��ˮ��Һ��ȫ��Ӧ
������뺬3mol NaOH��ˮ��Һ��ȫ��Ӧ
C.����ʽΪ![]() �IJ���ͬ���칹���п��ܺ��������ṹ��Ԫ
�IJ���ͬ���칹���п��ܺ��������ṹ��Ԫ
D.DDT�Ľṹ��ʽΪ��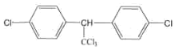 �����������13��̼ԭ�ӹ�ƽ��
�����������13��̼ԭ�ӹ�ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ����2C(s)��O2(g)![]() 2CO(g) ��H��221kJ��mol1����H��(aq)��OH(aq)
2CO(g) ��H��221kJ��mol1����H��(aq)��OH(aq)![]() H2O(l) ��H��57.3kJ��mol1�����н��۴������
H2O(l) ��H��57.3kJ��mol1�����н��۴������
A.̼��ȼ���ȴ���110.5kJ��mol1
B.�ٵķ�Ӧ��Ϊ221kJ��mol1
C.ϡ�����ϡNaOH��Һ��Ӧ����1mol H2O���ų�57.3kJ������
D.ϡH2SO4��ϡNaOH��Һ��Ӧ���к���Ϊ57.3kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������Һ��ķ�Ӧ��������ͬһ���ӷ���ʽ��ʾ���ǣ� ��
A.HCl��Na2CO3��HCl+NaHCO3B.BaCl2��Na2SO4��Ba(OH)2��H2SO4
C.ʯ��ʯ�����ᡢʯ��ʯ������D.KOH��HCl��Ba(OH)2��H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ7.90g KMnO4�����ȷֽ��ʣ�����7.42g����ʣ�������������Ũ�����ڼ��������³�ַ�Ӧ�����ɵ�������A����������Ԫ��ֻ��Mn2+���ڡ�����˵���д�����ǣ� ��
A.��Ӧ�������������������ʵ�����0.015mol
B.����A���������������ʵ�����0.095mol
C.KMnO4�ķֽ�����60%
D.������Ӧ������ת����0.19mole-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com