
����Ŀ����18molL��1Ũ��������100mL3.0molL��1ϡ�����ʵ�鲽�����£�
�ټ�������Ũ��������������ȡһ�������Ũ������ܽ⣻����ȴ����ת�ơ�ϴ�ӣ������ݡ�ҡ�ȣ� ��װƿ����ǩ��
����������⣺
��1������Ũ���������� �� ��ȡŨ�������õ���Ͳ�Ĺ��������������ѡ��A��10mL��B��25mL��C��50mL��D��100mL����
��2���ڢ۲�ʵ��IJ����� ��
��3����������������Ƶ�ϡ����Ũ���к�Ӱ�죿���á�ƫ��ƫС������Ӱ�족��д��
A�����õ�Ũ���᳤ʱ��������ܷⲻ�õ���������
B������ƿ������ˮϴ�Ӻ������������ˮ��
C�����ù����ձ���������δϴ����
D������ʱ���ӿ̶��� ��
���𰸡�
��1��16.7mL,B
��2�������ձ�����30mL��������������ˮ,Ȼ��Ũ�������ձ��ڱڻ��������ձ���,���ò���������
��3��ƫС,��Ӱ��,ƫС,ƫ��
���������⣺��1����Һϡ��ǰ�����ʵ����ʵ������䣬����ҪŨ��������ΪV��18molL��1��V�T100mL��3.0molL��1�����V=16.7ml��Ӧѡ��25ml����Ͳ��
��2��ϡ��Ũ����Ӧ��Ũ��������ע��ˮ�У������Ͻ��裬��ֹ�Ž���
��3���������ʵ���Ũ�ȶ���C= ![]() ����������ʹ���ʵ���nƫС����ʹVƫ��IJ�������ʹ��Һ�����ʵ���Ũ��ƫС����֮����Һ�����ʵ���Ũ��ƫ��
����������ʹ���ʵ���nƫС����ʹVƫ��IJ�������ʹ��Һ�����ʵ���Ũ��ƫС����֮����Һ�����ʵ���Ũ��ƫ��
A��Ũ���������ˮ�ԣ����õ�Ũ���᳤ʱ��������ܷⲻ�õ������У�Ũ�����Ũ�ȱ�ϡ��ʵ����ȡ��Ũ������������������ʵ���ƫС��������Һ��Ũ��ƫС��
B����Һ�������ˮ���ݣ�����ƿ������ϴ�Ӻ������������ˮ����������ҺŨ����Ӱ�죻
C�����ù����ձ���������δϴ�ӣ���������մ���ձ��ڡ��������ϣ���������ƿ����������ʵ������٣�������ҺŨ��ƫС��
D������ʱ���ӿ̶��ߣ�����Һ���ڿ̶������£���Һ�����ƫС��������Һ��Ũ��ƫ��
�ʴ�Ϊ����1��16.7mL��B����2�������ձ�����30mL ��������������ˮ��Ȼ��Ũ�������ձ��ڱڻ��������ձ��У����ò��������裻��3��ƫС����Ӱ�죻ƫС��ƫ��
��1����Ũ��Һ����ϡ��Һ��һ�����ϡ�Ͳ�����ϡ�����У����ʵ������ֲ������ݹ�ʽ![]() ���м��㣻��Ͳ��ȡ��Ӧ�������õ���Һ���������Ͳ�����̡�
���м��㣻��Ͳ��ȡ��Ӧ�������õ���Һ���������Ͳ�����̡�
��2��Ũ�����ϡ��Ӧ��Ũ�������ձ�������ע��ˮ�У������Ͻ��衣
��3��A.Ũ���������ˮ�ԣ����ڳ��ڷ��ú������Ũ���ᣬ���е����ʵ�����С��
B.����ƿ�ײ���ˮ����Ӱ����Һ�����ƣ�
C.�ձ�������������մ����Һ��δϴ�ӻᵼ�����ʱ��٣�
D.���ӿ̶��ߣ�ʵ��Һ�������С�ڿ̶��ߣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ�òⶨˮ���⡢��Ԫ�ص������ȣ��䷽���Ƿֱ�ⶨͨ����ǰ�����ܵ��������U�ܵ������ʵ����m��H����m��O����1��8�����жԵ�����һ�����ԭ��ķ����У�һ��������ǣ�������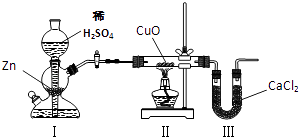
A.��װ��֮��ȱ�ٸ���װ��
B.��װ�ú�ȱ�ٸ���װ��
C.��װ���в���������ˮ����
D.CuOû��ȫ������ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�����жϳ��������ӷ���ʽ�д�����ǣ�������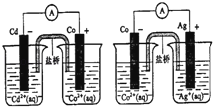
A.2Ag+��aq��+Cd��s��=2Ag��s��+Cd 2+��aq��
B.Co2+��aq��+Cd��s��=Co��s��+Cd2+��aq��
C.2Ag��s��+Cd2+��aq��=2Ag+��aq��+Cd��s��
D.2Ag+��aq��+Co��s��=2Ag��s��+Co2+��aq��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ͼ��ʾԭ��ص���������ȷ���ǣ�������װ�к�������KCl������Һ����������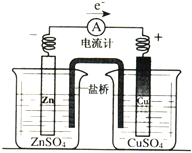
A.��Ӧ�У������е�K+������CuSO4��Һ
B.ȡ�����ź�������Ȼ����ƫת
C.ͭƬ���������ݳ�
D.��Ӧǰ��ͭƬ�������ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������m gij���壬������ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM gmol��1 �� ��
��1������������ʵ���Ϊmol��
��2����������������ԭ������Ϊ����
��3���������ڱ�״���µ����ΪL��
��4������������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ ��
��5������������ˮ���γ�V L��Һ������Һ�����ʵ���Ũ��ΪmolL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ÿ���ģ�����ĵ绯ѧ����������˵������ȷ���ǣ�������
A.��XΪп��������K����M�����ɼ������ĸ�ʴ
B.��XΪп��������K����M������������������Ӧ
C.��XΪ̼��������K����N�����ɼ������ĸ�ʴ
D.��XΪ̼��������K����N����X������������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Mg��Ͷ��ʢ��ϡHCl�����������H2���������������أ�������Ũ�� ���¶� ��þ���ı���� ���������ܱ���� ����Һ��c��Cl������С���й�ϵ���ǣ� ��
A.�٢�
B.�ۢ�
C.�٢ڢۢ�
D.�٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20�� ʱ��PbCl2��s���ڲ�ͬŨ�������е�����ܽ�������λ��gL��1����ͼ��ʾ������������ȷ���ǣ� �� 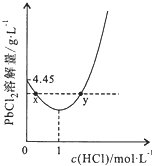
A.����Ũ��Խ��Ksp��PbCl2��Խ��
B.PbCl2����һ��Ũ�ȵ����ᷴӦ
C.x��y�����Ӧ����Һ��c��Pb2+�����
D.����Pb2+����Һ�м������Ũ���ᣬ�ɽ�Pb2+��ȫת��ΪPbCl2��s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��ز�����ɻ�����Ⱦ����
A. п�̵��B. ����ȼ�ϵ��C. ���ӵ��D. Ǧ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com