
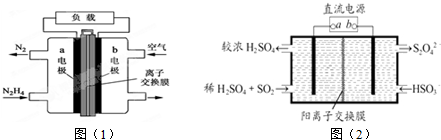
| A. | 图(1)中的a电极应与 图(2)的a相连 | |
| B. | 图(1)中a电极应的反应方程式为:N2H4+4OH--4e-═N2+4H2O | |
| C. | 用该燃料电池作为装置图(2)的直流电,吸收1 molSO2至少需要通人 0.5 mol N2H4 | |
| D. | 图(1)中OH-由阴离子交换膜从左流向右,图(2)中H+由阳离子交换膜从右流向左 |
分析 A、图(1)中的a电极肼发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,而图2中a二氧化硫发生氧化反应生成硫酸,发生氧化反应是阳极;
B、图(1)中的a电极肼发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O;
C、吸收1 molSO2转移2mol的电子,而1molN2H4转移4mol的电子;
D、原电池中阴离子向负极移动,电解池中的阳离子向阴移动.
解答 解:A、图(1)中的a电极肼发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,而图2中a二氧化硫发生氧化反应生成硫酸,发生氧化反应是阳极,阳与电源的正极相连,故A错误;
B、图(1)中的a电极肼发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,故B正确;
C、吸收1 molSO2转移2mol的电子,而1molN2H4转移4mol的电子,所以根据转移电子数目相等,则吸收1 molSO2至少需要通人 0.5 mol N2H4,故C正确;
D、原电池中阴离子向负极移动,所以图(1)是原电池,左侧是负极,OH-由阴离子交换膜从右流向左;电解池中的阳离子向阴移动,所以图(2)为电解池,左侧是阳极,H+由阳离子交换膜从左流向右,故D错误;
故选AD.
点评 本题考查了燃料电池,明确正负极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质溶液的酸碱性书写,注意电子不能在溶液中移动,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 物质的分离提纯方法之一为“筛分”:如胶体-渗析法提纯;悬浊液-过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的“筛子” | |
| B. | 酸式滴定管,碱式滴定管、移液管都是准确量取一定体积液体的仪器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 | |
| C. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3次的实验平均值等措施,已达到良好的实验结果 | |
| D. | 将适量植物油、酒精和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可以制得肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 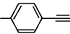 分子中所有原子在同一平面 分子中所有原子在同一平面 | |
| B. | 2,2-二甲基丙烷的核磁共振氢谱有1组峰 | |
| C. | 石油裂解、煤的干馏、玉米制醇、焰色反应都是化学变化 | |
| D. | 将淀粉在酸性条件下水解后直接加入银氨溶液,水浴加热,检验葡萄糖的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
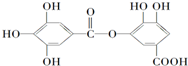
| A. | 在一定条件下,1 mol该物质最多能与6 mol NaOH完全反应 | |
| B. | 有弱酸性,1 mol该有机物与溴水反应,最多能消耗4 mol Br2 | |
| C. | 在Ni催化下,1 mol该物质可以和7 mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com