
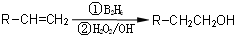
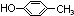 .
. .
.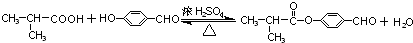 .
.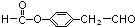 (邻、间、对任写一种即可).
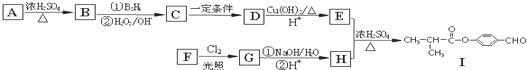
(邻、间、对任写一种即可). 分析 A为丁醇且核磁共振氢谱有2种不同化学环境的氢,则A为(CH3)3COH,A在浓硫酸、加热条件下发生消去反应生成B为CH2=C(CH3)2,B发生信息2中的反应生成C为(CH3)2CHCH2OH,C在Cu或Ag、加热条件下发生催化氧化生成D为(CH3)2CHCHO,D再与氢氧化铜反应,发生氧化反应,再酸化得到E为(CH3)2CHCOOH,由I的结构可知,H为 ,逆推可知G为
,逆推可知G为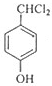 ,F为
,F为 ,符合F的分子式为C7H8O,苯环上的一氯代物只有两种的条件,F发生取代反应生成G,G碱性水解,发生取代反应生成H,据此分析解答.
,符合F的分子式为C7H8O,苯环上的一氯代物只有两种的条件,F发生取代反应生成G,G碱性水解,发生取代反应生成H,据此分析解答.
解答 解:A为丁醇且核磁共振氢谱有2种不同化学环境的氢,则A为(CH3)3COH,A在浓硫酸、加热条件下发生消去反应生成B为CH2=C(CH3)2,B发生信息2中的反应生成C为(CH3)2CHCH2OH,C在Cu或Ag、加热条件下发生催化氧化生成D为(CH3)2CHCHO,D再与氢氧化铜反应,发生氧化反应,再酸化得到E为(CH3)2CHCOOH,由I的结构可知,H为 ,逆推可知G为
,逆推可知G为 ,F为
,F为 ,符合F的分子式为C7H8O,苯环上的一氯代物只有两种的条件,F发生取代反应生成G,G碱性水解,发生取代反应生成H,
,符合F的分子式为C7H8O,苯环上的一氯代物只有两种的条件,F发生取代反应生成G,G碱性水解,发生取代反应生成H,
(1)通过以上分析知,B分子式为C4H8,
故答案为:C4H8;
(2)A发生消去反应生成B,C发生氧化反应生成D,故答案为:消去反应;氧化反应;
(3)芳香族化合物F的分子式为C7H8O,说明含有苯环,苯环上的一氯代物只有两种,说明苯环上只有2种氢原子,则其结构简式为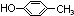 ,故答案为:
,故答案为: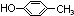 ;
;
(4)D生成E的化学方程式为: ,E与H反应生成I的方程式为:
,E与H反应生成I的方程式为: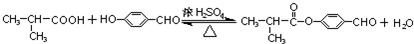 ,
,
故答案为: ;
; ;
;
(5)I( )的同系物K比I相对分子质量小28,则K比I少2个-CH2-原子团,K的结构中能同时满足如下条件:①苯环上只有两个取代基;②分子中不含甲基,
)的同系物K比I相对分子质量小28,则K比I少2个-CH2-原子团,K的结构中能同时满足如下条件:①苯环上只有两个取代基;②分子中不含甲基,
侧链为-CHO、-CH2OOCH或-CH2CHO、-OOCH二种结构,各有邻、间、对三种位置,故有6种,上述同分异构体中任意一种消耗NaOH最多的有机物结构简式为: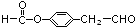 (邻、间、对任写一种即可)等,
(邻、间、对任写一种即可)等,
故答案为:6;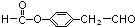 (邻、间、对任写一种即可).
(邻、间、对任写一种即可).
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识迁移能力,根据反应条件、题给信息、产物的结构简式进行推断,正确推断物质结构简式是解本题关键,难点是(5)题限制型同分异构体种类判断,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2CO3 BaCl2 NaOH | B. | CaC12 HCl KNO3 | ||
| C. | KOH HCl (NH4)2SO4 | D. | Fe2O3 KCl NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 购物时用布袋代替塑料袋 | B. | 农田过量施用农药、化肥 | ||
| C. | 工厂的废水经处理后再排放 | D. | 城市推广使用氢燃料电池客车 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com