
ʵ������������������Ʊ��������������й����ʵ�����������±���
| ������ | ��Է������� | �ܶ�/g��cm-3 | �е�/�� | �ܽ��/100gˮ |
| ������ | 74 | 0. 80 | 118.0 | 9 |
| ������ | 60 | 1.045 | 118.1 | ���� |
| ���������� | 116 | 0.882 | 126.1 | 0.7 |
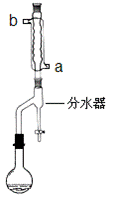 ��һ���������������Ʊ�
��һ���������������Ʊ�
���ڸ����50mLԲ����ƿ�У�����13.5mL��������7.2mL�����ᣬ�ټ���3��4��Ũ���ᣬҡ�ȣ�Ͷ��1��2����ʯ��Ȼ��װ��ˮ��(���ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ)���¶ȼƼ����������ܣ���������������Ӧ
��������Ʒ�ľ���
�ڽ���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У���10 mL��ˮϴ�ӡ��л��������10 mL10%Na2CO3ϴ�������ԣ�����10 mL ��ˮϴ�ӣ�����л���ת������ƿ�У�������ˮ����þ���
�۽���������������������50 mL ��ƿ�У���ѹ�����ռ�125��127 �����֣���11.6 g����������
��ش��й����⡣
��1����ˮӦ�ô������� ___________����a��b���ܿ�ͨ�롣
��2��������в��ϴӷ�ˮ���²��ֳ����ɵ�ˮ��Ŀ����_________________________
��������жϷ�Ӧ�յ��������_____________________________________��
 ��3����Ʒ�ľ��ƹ��̲�����У���һ��ˮϴ��Ŀ����_____________________________���ñ���Na2CO3��Һϴ���л��㣬�ò�������Ŀ����_________________________________��
��3����Ʒ�ľ��ƹ��̲�����У���һ��ˮϴ��Ŀ����_____________________________���ñ���Na2CO3��Һϴ���л��㣬�ò�������Ŀ����_________________________________��
��4�����й��ڷ�Һ©����ʹ��������ȷ����____
A����Һ©��ʹ��ǰ����Ҫ��©��ֻҪ��Һ©��������о����©ˮ����ʹ��
B��װҺʱ����Һ©����Һ�����������ó������ݻ���2/3
C����ȡ����Ӧ����ͼ��ʾ
D���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С��
��5������۵ij�ѹ�������ռ�126�����֣��е����140����л������������һ�㲻�����������ܶ��ÿ��������ܣ�����ԭ����_________________________
��6����ʵ������У�����������������ʽ��116���IJ�����__________
��֪ʶ�㡿����ʵ��������衢ʵ�鷽������������ۡ������Ʊ�
���𰸽����� ��1�� a ��1�֣� ��2��ʹ�÷�ˮ�������ˮ��ʹƽ�������ƶ�����߷�Ӧ���ʣ���2�֣� ��ˮ���е�ˮ�㲻������ʱ����Ϊ��Ӧ���յ㡣��2�֣�
��3����ȥ���ἰ����������������2�֣���ȥ��Ʒ�к��е���������ʡ���2�֣�
��4��D ��1�֣� ��5����ֹ���²����������ը�ѡ� ��2�֣�
��6�� 80% ��2�֣�
��������1����ˮҪ�������������ܾ�Ӧ�ô��������¹ܿ�ͨ�룻��2����Ϊ������Ӧ�ǿ��淴Ӧ�����Բ��ϴӷ�ˮ���²��ֳ����ɵ�ˮ������ʹƽ�������ƶ���������IJ��ʣ�����ˮ���е�ˮ�㲻������ʱ��˵����Ӧ�ﵽ�յ㣻��3����Ʒ�ľ��ƹ��̲�����У���ӦҺ�л������������������������һ��ˮϴ��Ŀ���dz�ȥ���ἰ���������������ñ���Na2CO3��Һϴ���л��㣬��ȥ��Ʒ�к��е���������ʣ���4����Һ©��ʹ��ʱע�����ʹ��ǰҪ�����������Ͽڴ��Ƿ�©ˮ����A����װ���Һ©����Һ���������Բ�Ҫ������Һ©���ݻ���12Ϊ�ˣ�װ��̫�����Һ��Ļ�ϣ���B������Һ��ʱҪ���÷�Һ©��������������Һ��Ļ�ϣ���C����Һʱ���ϲ�Һ����Ͽڵ������²�Һ�����¿ڷų������¿ڷų�Һ��ʱ��Ҫ���϶˲�������С�۶�������С��ʹ©��������ͨ����ʱ�رջ�������ֹ�ϲ�Һ����������D��ȷ����5���е����140����л������������һ�㲻��ˮ�����ܶ��ÿ��������ܣ���ֹ���²����������ը�ѡ���6��������������=0.8 g/mL��13.5mL=10.8g�������������=1.045g/mL��7.2mL=7.524g���ȸ��ݷ���ʽ�ж��������ʹ������Բ�������Ϊ�����м��㣮
������7.524g������ȫ��Ӧ������������Ϊxg������������������yg��
������������ķ�Ӧ����ʽΪ
CH3COOH+CH3CH2CH2CH2OH CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
60g 74g 116g 18g
7.524g yg xg
����x=14.5g y=9.3g��10.8g ���������������������������IJ���=11.6g��14.5g��100%=80%��
��˼·�㲦�����⿼�������Ʊ����Ƚ��ۺϣ�������ʵ��������裬��Ŀ�ѶȽϴ�ע����ػ���֪ʶ�Ļ��ۡ�


 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʳ���еĵ����Ե���أ�KIO3����ʽ���ڵġ���֪��������Һ��IO3-��I-�������з�Ӧ: IO3-+5I-+6H+=3I2+3H2O �����������ʢ�ϡ�����pH��ֽ���۵��۵⻯����Һ���ܵ�����Һ�� ����������Ӧ�����������麬��ʳ���к���IO3������ �� ��
A���ڢ� B���٢� C���ڢ� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ�������£����ڿ��淴ӦX(g)��3Y(g)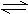 2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3(����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.08 mol��L��1���������ж���ȷ���ǣ� ��
2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3(����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.08 mol��L��1���������ж���ȷ���ǣ� ��
A��c1��ȡֵ��ΧΪ0 mol��L��1<c1<0.14 mol��L��1
B��ƽ��ʱ��Y��Z����������֮��Ϊ2��3
C��X��Y��ת���ʲ���� D��c1��c2��3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ӧm A��n B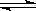 p C+q D��ij�¶��´ﵽƽ�⡣
p C+q D��ij�¶��´ﵽƽ�⡣
����A��B��C ��D�������壬�����¶Ȳ��䣬���������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱC�����ʵ���Ũ�ȱ�Ϊԭ����1.8������m��n��p ,q�Ĺ�ϵ��_____________��
����A��B��C ��D��Ϊ���壬��m+ n = p+ q�����������ѹ����A�����ʵ����� _________�����С�����������䡱��,ƽ��ض�______�ƶ������������������
��������ϵ���£� B�����ʵ������٣�������ӦΪ ________��Ӧ������ȡ������ȡ���
��������ϵ������A������ƽ�ⲻ�����ƶ�����A�϶�����Ϊ_____̬
����������������Ӧ���ת���ʽ�________�����С�����������䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ѪҺ�������Ҫ�����ƽ�⣺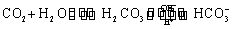 ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��
ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��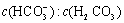 �仯��ϵ���±���
�仯��ϵ���±���
|
| 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.4 | 7.45 |
����˵������ȷ���ǣ� ��
A����������ѪҺ�У�HCO3����ˮ��̶ȴ��ڵ���̶�
B������ѪҺ���ж�ʱ����ע��NaHCO3��Һ����
C��pH=7.00��ѪҺ�У�c(H2CO3)��c(HCO3��)��
D��pH=7.40��ѪҺ�У�HCO3����ˮ��̶�һ������H2CO3�ĵ���̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ѧ��--ѡ��5���л���ѧ��������15�֣�
����Ȳ��Ϊԭ�Ͽɺϳ��л���H2MA������һ���ϳɸ߷��ӻ�����PMLA��
I������Ȳ�Ⱥϳ���C��
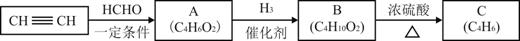
��֪��

��1��A�����еĹ�����������_______��_______��
��2��A��һ��ͬ���칹����������������ṹ��ʽ��________________
��3��Bת��ΪC�Ļ�ѧ����ʽ��________________________________________���䷴Ӧ������_______��
II������C�ϳ�PMLA��·�����¡�

��֪��

��4��1 mol�л���H������NaHCO3��Һ��Ӧ���ɱ�״���µ�CO2 44.8 L��H��˳���칹���䷴ʽ�ṹ��ʽ��________________
��5��E�Ľṹ��ʽ��________________
��6��G��NaOH��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ��_________________________
��7������PMLA�ж��ֽṹ��д����H2MA��PMLA�Ļ�ѧ����ʽ����дһ�֣�________________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A��ʯ�ͷ���ú����������ˮ��ʳ�Ρ������ʱ��Եȹ��̶�������ѧ�仯
B. ����������һ�����ܺ��ᷴӦ
C. ϡ���������ᡢ�Ȼ�����Һ��Ϊ����
D�������������ȼ��������������͡�����ϩ��Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��100mL 2mol��L��H2SO4������п�۷�Ӧ����һ���¶��£�Ϊ�˼�����Ӧ���ʶ���Ӱ������H2�����������ڷ�Ӧ���м���������
A. ����ͭ��Һ B.��������Һ C.��������Һ D.����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ӦN2��3H2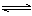 2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol��L��1��H2��Ũ��Ϊ5 mol��L��1��3 min����NH3Ũ��Ϊ0.6 mol��L��1�����ʱ����ڣ����з�Ӧ���ʱ�ʾ��ȷ����(����)
2NH3�տ�ʼʱ��N2��Ũ��Ϊ3 mol��L��1��H2��Ũ��Ϊ5 mol��L��1��3 min����NH3Ũ��Ϊ0.6 mol��L��1�����ʱ����ڣ����з�Ӧ���ʱ�ʾ��ȷ����(����)
A��v(NH3)��0.2 mol��L��1��s��1 B��v(N2)��1.0 mol��L��1��min��1
C��v(H2)��1.67 mol��L��1��min��1 D��v(H2)��0.3 mol��L��1��min��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com