
 P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:| A.加入一定量M | B.加入一定量N |
| C.反应温度升高 | D.缩小容器体积 |
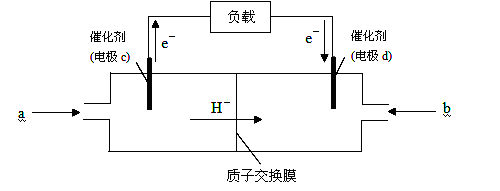
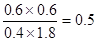 。
。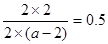 ,记得a=6。
,记得a=6。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
 H2(g) + I2(g)达到平衡状态的标志是:① I2的体积分数不再变化;② 生成1 mol H2同时消耗1 mol I2;③ 容器内压强不再变化;④ 生成2 mol HI同时消耗1 mol H2;⑤ 气体的密度不再变化;⑥ 混合气体的平均式量不再变化( )
H2(g) + I2(g)达到平衡状态的标志是:① I2的体积分数不再变化;② 生成1 mol H2同时消耗1 mol I2;③ 容器内压强不再变化;④ 生成2 mol HI同时消耗1 mol H2;⑤ 气体的密度不再变化;⑥ 混合气体的平均式量不再变化( )| A.①②③④⑤⑥ | B.①②③⑤⑥ | C.①②⑤⑥ | D.①② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 PCl5(g),达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g),达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量是( )| A.0.40mol | B.0.20mol | C.小于0.20mol | D.大于0.20mol,小于0.40mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。
CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。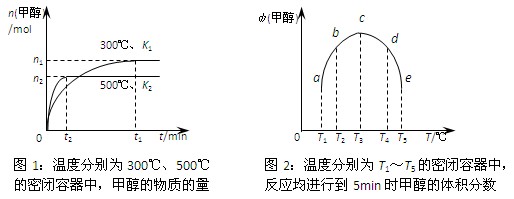
| A.该反应的正反应是气体体积减小的吸热反应 |
| B.K1<K2(K为该条件下反应的平衡常数) |
| C.反应进行到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动 |
| D.将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或减压 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 R(g)+S(g)在恒温下已达到平衡
R(g)+S(g)在恒温下已达到平衡| A.反应容器内的P、Q、R、S的浓度不随时间改变 |
| B.反应容器内P、Q、R、S四者共存 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g).能肯定该反应达到平衡状态的标志是( )
pC(g).能肯定该反应达到平衡状态的标志是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。 压强(MPa) 压强(MPa) 氨的含量 氨的含量温度(℃) | 0.1 | 10 | 30 | 60 | 100 |
| 200 | 0.153 | 0.815 | 0.899 | 0.954 | 0.988 |
| 300 | 0.022 | 0.520 | 0.710 | 0.842 | 0.926 |
| 400 | 0.004 | 0.251 | 0.470 | 0.652 | 0.798 |
 欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:
欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为: 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )| A.平衡向正反应方向移动 | B.物质A的转化率减小 |
| C.物质B的物质的量减少 | D.化学计量数a>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com