
| A. | 正常人血液内Kw=10-14 | |
| B. | 由题给数据可算得正常人血液的pH约为7.4 | |
| C. | 正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 当过量的碱进入血液中时,只发生HCO3-+OH-=CO32-+H2O的反应 |
分析 A.水的离子积与温度有关,人体正常体温为36.5℃,不是常温下;
B.根据Ka=$\frac{c(HC{{O}_{3}}^{-})•c({H}^{+})}{c({H}_{2}C{O}_{3})}$=10-6.1mol•L-1及正常血液中c(HCO3-):c(H2CO3)≈20:1计算出氢离子浓度;
C.根据溶液中的电荷守恒分析;
D.氢氧根离子能够与碳酸、碳酸氢根离子反应.
解答 解:A.常温下Kw=10-14,而正常人的体温为36.5℃,温度升高,水的离子积增大,则正常人血液内Kw>10-14,故A错误;
B.Ka=$\frac{c(HC{{O}_{3}}^{-})•c({H}^{+})}{c({H}_{2}C{O}_{3})}$,Ka=10-6.1mol•L-1,正常血液中c(HCO3-):c(H2CO3)≈20:1,则c(H+)=10-7.4mol•L-1,则pH=7.4,故B正确;
C.根据电荷守恒可知,c(HCO3-)+c(OH-)+2c(CO32-)=c(H+),故C错误;
D.碱能与碳酸反应,则当过量的碱进入血液中时,发生的反应有HCO3-+OH-=CO32-+H2O、H2CO3+2OH-=CO32-+2H2O,故D错误;
故选B.
点评 本题考查离子浓度大小比较、弱电解质的电离平衡及其影响,题目难度中等,明确题干信息及有关Ka的计算是解答本题的关键,注意掌握电离平衡常数的概念及计算方法,能够根据电荷守恒判断离子浓度大小.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
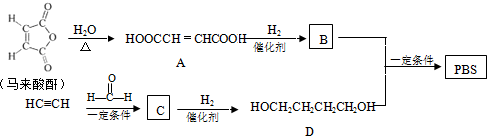
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 →CH≡CH的化学方程式(注明条件)
→CH≡CH的化学方程式(注明条件) +2NaOH$→_{△}^{乙醇}$CH≡CH+2NaBr+2H2O.
+2NaOH$→_{△}^{乙醇}$CH≡CH+2NaBr+2H2O. 和
和 合成CH3CH2CH2CH2OH的反应流程图(有机物用结构简式表示,必须注明反应条件).
合成CH3CH2CH2CH2OH的反应流程图(有机物用结构简式表示,必须注明反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| B. | MgO、Al2O3的熔点很高,可制作耐高温材料 | |
| C. | 二氧化硫具有漂白性,可用于漂白纸浆和草帽辫 | |
| D. | 铜盐能使蛋白质变性,游泳场馆常用硫酸铜作池水消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 硝基苯的结构简式: | |
| C. | (CH3 CH2)2 CHCH2CH3 的名称:2-乙基丁烷 | |
| D. | 甲基的电子式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
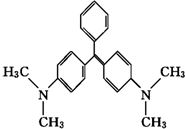 孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )| A. | 孔雀石绿的分子式为C23H25N2 | |
| B. | 1 mol孔雀石绿在一定条件下最多可与6 mol H2发生加成反应 | |
| C. | 孔雀石绿属于芳香族化合物 | |
| D. | 孔雀石绿苯环上的一氯取代物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32gO2和O3的混合气体所含原子数为2NA | |
| B. | 将7.1g氯气通入足量水中发生反应,所转移的电子数为0.1NA | |
| C. | 标准状况下,11.2LSO2中含有的分子数为0.5NA | |
| D. | 23g钠与足量氧气充分反应,转移的电子数一定是NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com