
| A£® | CH3COOHŌŚĖ®ÖŠµēĄė£ŗCH3COOHØTH++CH3COO- | |
| B£® | ŅŅ“¼Ńõ»Æ³ÉŅŅČ©µÄ»Æѧ·½³ĢŹ½£ŗ2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O | |
| C£® | ŅŅĖįÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦£ŗCH3COOH+CH3CH2OH$”ś_{”÷}^{“߻ƼĮ}$CH3COOCH2CH3 | |
| D£® | CaCO3øßĪĀ·Ö½āµÄČČ»Æѧ·½³ĢŹ½£ŗCaCO3$\frac{\underline{\;øßĪĀ\;}}{\;}$CaO+CO2”ü£¬”÷H=+178.5 kJ•mol-1 |
·ÖĪö A£®“×ĖįĪŖČõĖį£¬“ęŌŚµēĄėĘ½ŗā£»
B£®ŅŅ“¼Ńõ»Æ³ÉŅŅČ©£¬-OH×Ŗ»ÆĪŖ-CHO£»
C£®·¢Éśõ„»Æ·“Ӧɜ³ÉŅŅĖįŅŅõ„ŗĶĖ®£»
D£®ČČ»Æѧ·“Ó¦·½³ĢŹ½ÖŠ×¢Ć÷ĪļÖŹµÄדĢ¬£®
½ā“š ½ā£ŗA£®CH3COOHŌŚĖ®ÖŠµēĄė·½³ĢŹ½ĪŖCH3COOH?H++CH3COO-£¬¹ŹA“ķĪó£»
B£®ŅŅ“¼Ńõ»Æ³ÉŅŅČ©µÄ»Æѧ·½³ĢŹ½ĪŖ2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£¬ĪŖŃõ»Æ·“Ó¦£¬¹ŹBÕżČ·£»
C£®ŅŅĖįÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µÄ·½³ĢŹ½ĪŖCH3COOH+CH3CH2OH$”ś_{”÷}^{“߻ƼĮ}$CH3COOCH2CH3+H2O£¬¹ŹC“ķĪó£»
D£®CaCO3øßĪĀ·Ö½āµÄČČ»Æѧ·½³ĢŹ½ĪŖCaCO3£Øs£©$\frac{\underline{\;øßĪĀ\;}}{\;}$CaO£Øs£©+CO2£Øg£©”÷H=+178.5 kJ•mol-1£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó·“Ó¦¼°»Æѧ·“Ó¦µÄŹéŠ“£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ·¢ÉśµÄ·“Ó¦¼°Ąė×Ó·“Ó¦µÄŹéŠ“·½·ØĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ÄÉĆ×¼¶Cu2OÓÉÓŚ¾ßÓŠÓÅĮ¼µÄ“߻ƊŌÄܶųŹÜµ½¹Ų×¢£¬ĻĀ±ķĪŖÖĘČ”Cu2OµÄČżÖÖ·½·Ø£ŗ
ÄÉĆ×¼¶Cu2OÓÉÓŚ¾ßÓŠÓÅĮ¼µÄ“߻ƊŌÄܶųŹÜµ½¹Ų×¢£¬ĻĀ±ķĪŖÖĘČ”Cu2OµÄČżÖÖ·½·Ø£ŗ| ·½·ØI | ÓĆĢ¼·ŪŌŚøßĪĀĢõ¼žĻĀ»¹ŌCuO |
| ·½·ØII | ÓĆėĀ£ØN2H4£©»¹ŌŠĀÖĘCu£ØOH£©2 |
| ·½·ØIII | µē½ā·Ø£¬·“Ó¦ĪŖ2Cu+H2O$\frac{\underline{\;µē½ā\;}}{\;}$Cu2O+H2”ü |
| ŠņŗÅ | Cu2O aæĖ | ĪĀ¶Č | 0 | 10 | 20 | 30 | 40 | 50 |
| ¢Ł | ·½·ØII | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ¢Ś | ·½·ØIII | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ¢Ū | ·½·ØIII | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ē½šŹōŠŌ£ŗY£¼X£¼W | |
| B£® | ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗY£¼X | |
| C£® | »ÆŗĻĪļZW”¢XYÖŠ»Æѧ¼üĄąŠĶĻąĶ¬ | |
| D£® | X”¢WµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¾łĪŖĒæĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
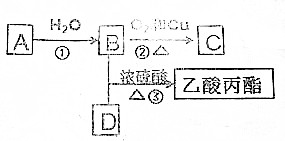
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼Ō×Ӽ䶼ŅŌµ„Į“ĻąĮ¬µÄĮ“ĢžŹĒĶéĢž | |
| B£® | ĖłÓŠĢĒĄąĪļÖŹ¶¼ÓŠĢšĪ¶ | |
| C£® | ÓĶÓėÖ¬·¾¶¼ŹōÓŚøŹÓĶõ„ | |
| D£® | ĘĻĢŃĢĒÓė¹ūĢĒ»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃé²Ł×÷ | ĻÖĻó | ½įĀŪ | |
| A | ĻņŹ¢ÓŠ25mL·ŠĖ®µÄÉÕ±ÖŠµĪ¼Ó5”«6µĪFeCl3±„ŗĶČÜŅŗ£¬¼ĢŠųÖó·Š | ČÜŅŗÉś³ÉŗģŗÖÉ«³Įµķ | ÖʵĆFe£ØOH£©3½ŗĢå |
| B | ĻņĮ½Ö§Ź¢ÓŠKI3ČÜŅŗµÄŹŌ¹ÜÖŠ£¬·Ö±šµĪ¼Óµķ·ŪČÜŅŗŗĶAgNO3ČÜŅŗ£¬ | Ē°ÕßČÜŅŗ±äĄ¶£¬ ŗóÕßÓŠ»ĘÉ«³Įµķ | KI3ČÜŅŗÖŠ“ęŌŚĘ½ŗā£ŗ I3-?I2+I- |
| C | ½«äåŅŅĶéŗĶNaOHŅŅ“¼ČÜŅŗ»ģŗĻ¼ÓČČ£¬²śÉśĘųĢåĶØČėĖįŠŌKMnO4ČÜŅŗ | ĖįŠŌKMnO4ČÜŅŗ ĶŹÉ« | Ņ»¶Ø²śÉśĮĖŅŅĻ© |
| D | ŌŚµĪÓŠ·ÓĢŖµÄNa2CO3ČÜŅŗÖŠ£¬¼ÓČėCaCl2ČÜŅŗ | ČÜŅŗĶŹÉ« | CaCl2ČÜŅŗÓŠĖįŠŌ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż |
| c£ØI-£©/mol/L | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c£ØS2O${\;}_{8}^{2-}$£©/mol/L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
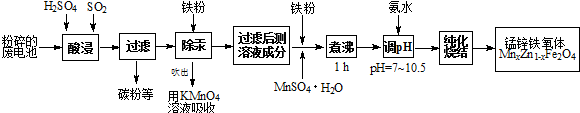
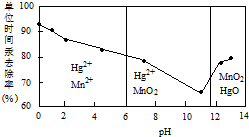
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ĪŹĢā | ĘĄ¼Ū |
| A | ÓĆĻ”ĻõĖįĒåĻ“×ö¹żŅų¾µ·“Ó¦µÄŹŌ¹Ü Ag+4H++NO3-=Ag++NO”ü+2H2O | “ķĪó£¬ĪļÖŹ²š·Ö“ķĪó |
| B | Ąė×Ó×é Na+”¢K+”¢HCO3-”¢OH- | ²»ÄÜ“óĮæ¹²“ęÓŚĶ¬Ņ»ČÜŅŗÖŠ£¬ŅņĪŖ·¢Éś·“Ó¦£ŗ HCO3-+OH-=H2O+CO2”ü |
| C | ·“Ó¦£ŗ Cu2+£Øaq£©+MnS£Øs£©?CuS£Øs£©+Mn2+£Øaq£© | øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½£ŗK=$\frac{{K}_{sp}£ØMnS£©}{{K}_{sp}£ØCuS£©}$ |
| D | ŌŚĮņĖįĒāÄĘČÜÓŚĖ®µÄ¹ż³ĢÖŠ | Ö»ÓŠĄė×Ó¼ü±»ĘĘ»µĆ»ÓŠ¹²¼Ū¼ü±»ĘĘ»µ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com