
【题目】C、S和Cl元素的单质及化合物在工业生产中的有效利用备受关注。请回答下列问题:
(1)已知:Ⅰ.2SO2(g)+O2(g)+2H2O(l)=2H2SO4(aq)ΔH1;
Ⅱ.Cl2(g)+H2O(l)![]() HCl(aq)+HClO(aq)ΔH2;
HCl(aq)+HClO(aq)ΔH2;
Ⅲ.2HClO(aq)=2HCl(aq)+O2(g)ΔH3;
SO2(g)+Cl2(g)+2H2O(l)=2HCl(aq)+H2SO4(aq)
ΔH4=____________________(用含有ΔH1、ΔH2和ΔH3的代数式表示)。
(2)25℃时,H2SO3溶液中各含硫微粒的物质的量分数(δ)与溶液pH的变化关系如图甲所示。
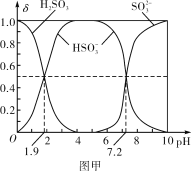
已知25℃时,NaHSO3的水溶液pH<7,用图中的数据通过计算解释原因_____________________________________________________。
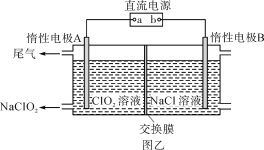
(3)NaClO2是一种绿色消毒剂和漂白剂,工业上采用电解法制备NaClO2的原理如图乙所示。
①交换膜应选用____________________(填“阳离子交换膜”或“阴离子交换膜”)。
②阳极的电极反应式为_____________________________________。
(4)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,发生反应2CO(g)+SO2(g)![]() S(l)+2CO2(g)ΔH=-270kJ/mol,若反应进行到20min时达到平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=______________,该温度下化学平衡常数K=____________(L·mol-1)
S(l)+2CO2(g)ΔH=-270kJ/mol,若反应进行到20min时达到平衡,测得CO2的体积分数为0.5,则前20min的反应速率v(CO)=______________,该温度下化学平衡常数K=____________(L·mol-1)
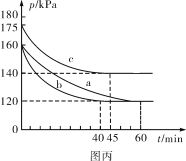
(5)在不同条件下,向2L恒容密闭容器中通入2molCO和1molSO2,反应体系总压强随时间的变化如图丙所示:
①图丙中三组实验从反应开始至达到平衡时,v(CO)最大的为__________(填字母序号)。
②与实验a相比,c组改变的实验条件可能是_____________________________________。
【答案】![]() 由图中数据可以计算出Ka2(H2SO3)=10-7.2,Ka1(H2SO3)=10-1.9,
由图中数据可以计算出Ka2(H2SO3)=10-7.2,Ka1(H2SO3)=10-1.9,![]() 的水解常数是10-12.1,
的水解常数是10-12.1,![]() 电离程度大于水解程度,溶液显酸性 阳离子交换膜 2Cl--2e-===Cl2↑ 0.03mol·L-1·min-1 11.25 b 升高温度
电离程度大于水解程度,溶液显酸性 阳离子交换膜 2Cl--2e-===Cl2↑ 0.03mol·L-1·min-1 11.25 b 升高温度
【解析】
(1)利用盖斯定律同向相加,异向相减的原则计算ΔH4=![]() ;
;
(2)根据图像pH=1.9时,Ka1(H2SO3)=![]() =10-1.9,则HSO3-的水解平衡常数Kh=
=10-1.9,则HSO3-的水解平衡常数Kh=![]() =10-12.1,根据pH=7.2,计算Ka2=c(H+)=10-7.2,然后比较
=10-12.1,根据pH=7.2,计算Ka2=c(H+)=10-7.2,然后比较![]() 电离程度与HSO3-的水解程度的大小,确定溶液酸碱性;
电离程度与HSO3-的水解程度的大小,确定溶液酸碱性;
(3)分析图像中的反应物和产物,可以看出左侧由ClO2制备NaClO2,需要Na+从右侧到左侧,所以判定交换膜为阳离子交换膜;
(4)根据已知条件,列“三段式”:根据平衡时CO的体积分数,计算出平衡CO、SO2、CO2的物质的量浓度,计算出平衡常数;
(5)根据反应前后单位时间内总压强的变化,比较反应速率的快慢。
(1)Ⅰ.2SO2(g)+O2(g)+2H2O(l)=2H2SO4(aq)ΔH1;Ⅱ.Cl2(g)+H2O(l)![]() HCl(aq)+HClO(aq) ΔH2;Ⅲ.2HClO(aq)=2HCl(aq)+O2(g) ΔH3;由盖斯定律:
HCl(aq)+HClO(aq) ΔH2;Ⅲ.2HClO(aq)=2HCl(aq)+O2(g) ΔH3;由盖斯定律:![]() ×(Ⅰ+Ⅱ×2+Ⅲ) 得,SO2(g)+Cl2(g)+2H2O(l)=2HCl(aq)+H2SO4(aq) ΔH4=
×(Ⅰ+Ⅱ×2+Ⅲ) 得,SO2(g)+Cl2(g)+2H2O(l)=2HCl(aq)+H2SO4(aq) ΔH4=![]() ;
;
(2)由图中的数据计算的H2SO3电离平衡常数Ka1、Ka2,当pH=7.2时,c(HSO3-)=c(SO32-),Ka2=![]() =c(H+)=10-7.2;当pH=1.9时,c(HSO3-)=c(H2SO3),Ka1=
=c(H+)=10-7.2;当pH=1.9时,c(HSO3-)=c(H2SO3),Ka1=![]() =10-1.9,所以HSO3-的水解平衡常数= Kh=
=10-1.9,所以HSO3-的水解平衡常数= Kh=![]() =10-12.1
=10-12.1![]() 电离程度大于水解程度,NaHSO3的水溶液显酸性,NaHSO3溶液的pH<7;
电离程度大于水解程度,NaHSO3的水溶液显酸性,NaHSO3溶液的pH<7;
(3)①由ClO2 →NaClO2可知,氯元素的化合价降低,所以ClO2得到电子发生还原反应,即A电极为阴极,电极反应式为ClO2 +e-=ClO2-,ClO2-结合Na+生成NaClO2,所以Na+由阳极区移向阴极区,则离子交换膜为阳离子交换膜;
②阳极区Cl-失去电子生成氯气,电极反应式为2Cl--2e-===Cl2↑;
(4)令反应中二氧化硫的变化量为x mol/L,根据化学方程式方程式,列出反应的三段式:
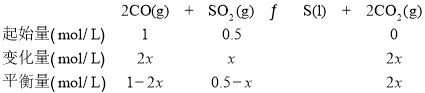
由于二氧化碳的体积分数为0.5,则![]() ,x=0.3,所以v(CO)=
,x=0.3,所以v(CO)=![]() =0.03mol·L-1·min-1;平衡常数:
=0.03mol·L-1·min-1;平衡常数:![]() ;
;
(5)①实验c由175kPa起始,达到平衡所需时间为455min,实验a与实验b相比,所以b达到平衡所用的时间更短,单位时间内总压强的变化分别为,实验b:
![]() ,实验c:
,实验c:![]() ,所以实验b的反应速率更快,即v(CO)最大的为b;
,所以实验b的反应速率更快,即v(CO)最大的为b;
②与实验a相比,实验c达到平衡所需时间更短,所以速率加快,根据反应方程式2CO(g)+SO2(g)![]() S(l)+2CO2(g)ΔH=-270kJ/mol,改变条件后,压强增大,说明平衡向逆反应方向移动,因为该反应的正反应是放热反应,故改变的条件可能是升高温度。
S(l)+2CO2(g)ΔH=-270kJ/mol,改变条件后,压强增大,说明平衡向逆反应方向移动,因为该反应的正反应是放热反应,故改变的条件可能是升高温度。
【点晴】
在比较弱酸的酸式盐的溶液呈酸性或碱性时,考生应结合题中图像信息,找到关键的几个特殊点,计算出电离平衡常数和水解平衡常数,如果弱酸的酸式根离子的电离平衡常数大于弱酸的酸式根离子的水解平衡常数,则溶液呈酸性;若弱酸的酸式根离子的电离平衡常数小于弱酸的酸式根离子的水解平衡常数,则溶液呈碱性。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,将1.0L c mol·L-1 CH3COOH溶液与0.1mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述错误的是( )
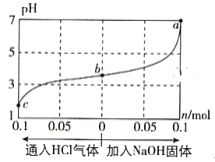
A. 水的电离程度:a>b>c
B. c点对应的混合溶液中:c(CH3COOH)>c(Na+)>c(OH-)
C. a点对应的混合溶液中:c(Na+)=c(CH3COO-)
D. 该温度下,CH3COOH的电离平衡常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每次取20 g海水,严格按照过滤、蒸发、冷却、称量、计算的实验步骤规范操作,连续实验三次,平均得固态盐a g。该海水中含氯化钠的质量分数是( )
A.大于5a%
B.小于5a%
C.等于5a%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 实验室可以用排饱和食盐水的方法收集氯气
B. 将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快
C. 高压有利于工业上合成氨
D. 打开汽水瓶时,瓶中立即泛起大量泡沫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法标出下列反应电子转移的方向和数目。
(1)4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O_________________
MnCl2+Cl2↑+2H2O_________________
(2)2KClO3![]() 2KCl+3O2↑__________
2KCl+3O2↑__________
(3)Cl2+2NaOH===NaClO+NaCl+H2O__________
(4)2H2O2![]() 2H2O+O2↑__________
2H2O+O2↑__________
(5)S+2H2SO4(浓)![]() 3SO2↑+2H2O__________
3SO2↑+2H2O__________
(6)6HCl+KClO3===3Cl2↑+KCl+3H2O__________
(7)3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O__________
(8)2KMnO4![]() K2MnO4+MnO2+O2↑__________
K2MnO4+MnO2+O2↑__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用海水制备金属镁的流程如图所示,请据图回答下列问题:
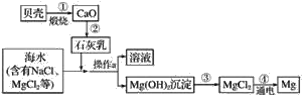
(1)贝壳主要成分的化学式是__。
(2)第②步是用生石灰和水反应制取石灰乳(主要成分是氢氧化钙)请写出制取石灰乳的化学方程式:__,基本反应类型是__。
(3)第③步是将沉淀出的氢氧化镁与盐酸反应生成氯化镁,写出该反应的化学方程式:__,该反应基本类型是__。
(4)第④步是无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式:___,反应基本类型是__。
(5)要使海水中MgCl2完全转化为沉淀Mg(OH)2,加入石灰乳的量应过量,确定海水中的MgCl2已全部转化为Mg(OH)2的方法:取上层清液少量,向其中加入氢氧化钠溶液,观察到__。
(6)海水中本来就有氯化镁,请分析从海水中制取MgCl2时,要经历“MgCl2→Mg(OH)2→MgCl2”的转化原因:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2SO2(g)+O2(g)![]() 2SO3(g)在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
2SO3(g)在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
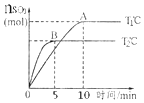
(1)反应后18O原子存在于哪些物质中___(填化学式)。
(2)上述反应的温度T1___ T2(填“>”“<”或“=”)。
(3)若温度T2时,5min后反应达到平衡,SO2的转化率为90%,则:
①平衡时体系内所含物质总的物质的量为___。
②平衡时SO3的浓度为___。
③下列说法不正确的是___。
A.如在该反应体系中加入适当的催化剂,可加快化学反应速率
B.其它条件相同时,该反应在T1时生成SO3的速率比T2时的小
C.该反应到达平衡时,体系内各组分的体积分数保持不变
D.若密闭容器中混合气体密度不变,则该反应达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.5 mol钠、0.5 mol镁分别放入20 mL 1 mol·L-1的盐酸中,下列说法正确的是( )
A.钠与盐酸反应比镁剧烈B.镁与盐酸反应比钠剧烈
C.反应结束时钠、镁都有剩余D.反应结束时产生的气体一样多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com