
【题目】【化学--有机化学基础】有机物G(![]() )是一种调香香精,可用作抗氧剂,工业上合成它的路线图之一如下:
)是一种调香香精,可用作抗氧剂,工业上合成它的路线图之一如下:

(1)A中官能团的名称是_____,B→C的反应类型为_________。
(2)G分子中一定共平面的碳原子有______个。
(3)反应F→G中消耗的F与CH3MgBr的物质的量之比为______,B在浓硫酸存在下加热可通过一步反应得到E物质,但合成不采用此方法,其原因是__________。
(4)C→D的化学方程式为_______________。
(5)E有多种同分异构体,其中满足下列条件的同分异构体有_____种,写出核磁共振氢谱有4个吸收蜂的物质的结构简式:_______。
①含有一个六元环 ②1mol同分异构体与足量银氨溶液发生银镜反应生成4 mol Ag
(6)已知A转化为B的原理与F转化为G的相似,请设计以A为起始原料(其他试剂任选)制备![]() 的合成路线______________。
的合成路线______________。
【答案】 羰基、羧基 取代反应 5 1:2 B可发生分子间(或分子内)酯化反应生成副产物 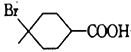 +2NaOH
+2NaOH![]() +NaBr+2H2O 4
+NaBr+2H2O 4 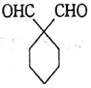 、
、 
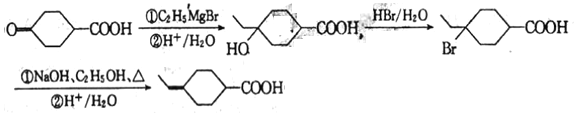
【解析】流程分析:B的分子式为C8H14O3,则B→C可表示为C8H14O3+HBr→C8H13O2Br,则B→C为醇羟基的卤代反应,C为![]() 。根据反应条件可知,C在NaOH醇溶液、加热的条件下发生消去反应生成D为
。根据反应条件可知,C在NaOH醇溶液、加热的条件下发生消去反应生成D为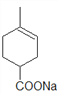 。酸化D得到E,则E为
。酸化D得到E,则E为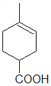 。E在浓硫酸加热的条件下,与乙醇发生消去反应生成F,则F为
。E在浓硫酸加热的条件下,与乙醇发生消去反应生成F,则F为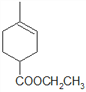 。
。
(1)根据A的结构简式可知,A中含有的官能团为:羰基、羧基。根据上述分析B→C为取代反应。故答案为:羰基、羧基;取代反应。
(2)G中碳碳双键为平面结构,与双键直接相连的碳原子(共3个)一定在同一平面内,则G分子中一定共平面的碳原子有5个。故答案为:5。
(3)根据反应条件可知,F→G与A→B反应类型相同。反应A→B中,羰基与CH3MgBr发生加成后,再水解得到D,最后羰基(C=O)中O原子上接H变-OH,C原子上接-CH3。反应F→G中,分析G的结构可知,F的羰基中O原子变-OH,C原子上连有2个-CH3,则1分子F应与2分子CH3MgBr反应,即消耗的F与CH3MgBr的物质的量之比为1∶2。B在浓硫酸存在下加热可发生消去反应生成E,但B中既含有-OH,又含有-COOH,在浓硫酸作用下可能发生分子内或分子间的酯化反应,故不采用此方法合成E。故答案为:1∶2;B可发生分子间(或分子内)酯化反应生成副产物。
(4)C→D为消去反应,反应方程式为:
![]()
![]()
![]() + NaBr +2H2O
+ NaBr +2H2O
(5)E为 。根据要求②可知,符合要求的同分异构体应含有2个-CHO,则除六元环外的2个C原子和2个O原子分别在-CHO中。则符合要求的同分异构体有以下4种:
。根据要求②可知,符合要求的同分异构体应含有2个-CHO,则除六元环外的2个C原子和2个O原子分别在-CHO中。则符合要求的同分异构体有以下4种:![]() 、
、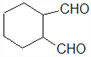 、
、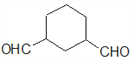 、
、![]() 。其中
。其中![]() 和
和 的核磁共振氢谱有4个吸收蜂。
的核磁共振氢谱有4个吸收蜂。
故答案为:4;![]() 、
、 。
。
(6)流程目的为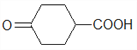 →
→ 。反应A→B中,
。反应A→B中,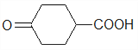 →
→![]() 。对比目标产物
。对比目标产物![]() 与B(
与B(![]() )的结构可知,目标产物比B多1个碳原子。则可利用A与CH3CH2MgBr发生类似“A→B”的反应,得到
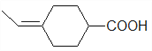
)的结构可知,目标产物比B多1个碳原子。则可利用A与CH3CH2MgBr发生类似“A→B”的反应,得到![]() 。为避免发生酯化反应,所以先发生类似“B→C”的取代反应得到
。为避免发生酯化反应,所以先发生类似“B→C”的取代反应得到![]() ,再消去即可得目标产物。故合成路线可表示如下:
,再消去即可得目标产物。故合成路线可表示如下:
![]()
![]()
![]()
![]()
![]()
![]()


科目:高中化学 来源: 题型:
【题目】为测定Cl2、Br2的氧化性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)。实验步骤如下图,填写图中的空白。
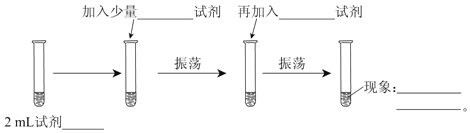
(1)2 mL试剂_______________;
(2)加入少量___________试剂;
(3)再加入___________试剂;
(4)现象_____________________________________________________。
(5)可以证明Cl2的氧化性____________(填强于、弱于)Br2的氧化性。
(6)发生反应的离子反应方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关离子浓度及pH大小的比较,正确的是( )
A. NH4+浓度相同的下列溶液:①(NH4)2Fe(SO4)2 ②(NH4)2CO3 ③(NH4)2SO4,溶液浓度由大到小的顺序是:③>②>①
B. 由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,其离子浓度不可能是:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C. pH=13的Ba(OH)2溶液与pH=1的HCl溶液等体积混合后,混合溶液的pH>7
D. pH=12的Ba(OH)2溶液与pH=14的NaOH溶液等体积混合,混合溶液的pH范围是13<pH<14
【答案】D
【解析】①(NH4)2Fe(SO4)2溶液中Fe2+的水解对于铵根离子的水解起到抑制作用, ②(NH4)2CO3 中碳酸根离子水解对于铵根离子的水解起到促进作用,③(NH4)2SO4溶液中硫酸根离子对铵根离子的水解无影响,所以溶液中铵根离子的水解程度的大小顺序为:②>③>①。则要达到相同的铵根离子浓度,水解程度大的溶液,物质的浓度应该越大,即溶液浓度由大到小的顺序是:②>③>①。选项A错误。由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,由于醋酸的浓度远大于氢氧化钠的浓度,所以中和以后得到醋酸钠(较少)和醋酸(较多)的混合溶液,溶液显酸性,即c(H+)>c(OH-),根据电荷守恒得到:c(CH3COO-)>c(Na+)。又因为钠离子是醋酸钠完全电离生成的,氢离子使醋酸微弱电离得到的,所以有c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。选项B错误。pH=13的Ba(OH)2溶液与pH=1的HCl溶液等体积混合,两溶液的氢氧根离子和氢离子的浓度刚好相等,等体积混合,恰好中和,溶液显中性。选项C错误。pH=12的Ba(OH)2溶液与pH=14的NaOH溶液等体积混合,其![]() ,所以
,所以![]() ,
, ![]() ,选项D正确。
,选项D正确。
【题型】单选题
【结束】
14
【题目】室温下,下列溶液中粒子浓度关系正确的是( )
A. Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4)
B. 20mL0.1molL-1CH3COONa溶液与10mL0.1molL-1HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
D. pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿(主要成分是Cu2S)含铜量高,是最重要的炼铜矿石。
I.已知: ①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ.mol-1
②Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H=-217.4kJ.mol-1
(1)Cu2S与Cu2O反应生成Cu和SO2的热化学方程式为_____________。
Ⅱ.Cu2O可催化二甲醚合成乙醇。
反应①:CH3OCH3(g)+CO(g)![]() CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g)+2H2(g)![]() CH3OH(g)+C2H5OH(g) △H2
CH3OH(g)+C2H5OH(g) △H2
(2)压强为pkPa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图1所示,则△H1____(填“>”或“<”,下同)0、△H2_____0。温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如图2所示。在300~600K范围内,乙酸甲酯的百分含量逐渐增大,而乙醇的百分含量逐渐减小的原因是____________。

(3)若压强为pkPa、温度为800K时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为_________,该条件下平衡常数K=_____________。
(4)以铜为原料,利用电解法可制取具有广泛用途的光电材料——纳米Cu2O,其工作原理如图3所示。则b是_______极,电解时阳极的电极反应式为______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A.平衡时,v正(O2)=v逆(O2)必成立
B.关系式5v正(O2)=4v正(NO)总成立
C.用上述四种物质NH3、O2、NO、H2O表示的正反应速率的数值中,v正(H2O)最小
D.若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
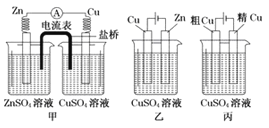
A. 甲是原电池,乙是电镀装置 B. 甲、乙装置中,锌极上均发生氧化反应
C. 乙、丙装置中,阳极均发生氧化反应而溶解 D. 丙装置中,铜电极的质量有增有减
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确为是( )
A.煤的干馏和液化均属于化学变化
B.铅蓄电池在放电过程中负极和正极的质量均增大
C.甲烷、乙烯和苯都不能使酸性高锰酸钾溶液褪色
D.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com