
【题目】下列关于金属物理性质的描述中,正确的是
A.金属钠的硬度很大B.铝易溶于水
C.铁是一种紫红色金属D.铁可以被磁铁吸引
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A. 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B. 28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C. 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
D. 常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 氢氧化钡溶液与足量硫酸氢钠的溶液混合:Ba2++OH―+H++SO42―=BaSO4↓+H2O
B. 过量的铁溶于稀硝酸:Fe+4H++NO3―=Fe3++NO↑+2H2O
C. 氯气与水:Cl2+H2O![]() 2H++Cl―+ClO―
2H++Cl―+ClO―
D. 硫酸铝溶液中加过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
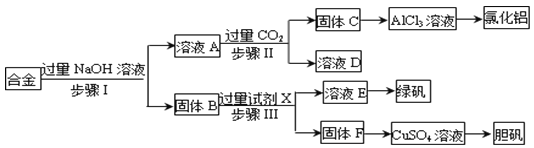
请回答:
(1)写出步骤Ⅰ反应的离子方程式:_________________________。
(2)试剂X是______。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是________。
(3)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式_______________________________,请选出你认为的最佳途径并说明选择的理由______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是
A. 用石墨作电极电解CuCl2溶液:2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B. 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C. 将少量二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O
D. Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关项目的比较中,错误的是
A.酸性:H2SiO3>H2CO3B.氧化性:Fe3+>Fe2+
C.热稳定性:Na2CO3>NaHCO3D.硬度:金刚石>刚玉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于烷烃的叙述不正确的是
A. 分子式符合CnH2n+2的烃一定是烷烃 B. 烷烃均能与氯水发生取代反应
C. 正丁烷的熔、沸点比异丁烷的高 D. 烷烃不能被酸性高锰酸钾溶液等强氧化剂氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生用如下图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物。
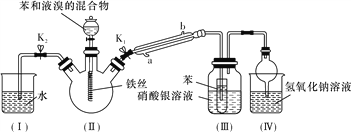
请回答下列问题:
(1)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。装置Ⅱ中生成有机物的反应为__________________________________________(填化学方程式),装置Ⅲ中小试管内苯的作用是__________________________________。
(2)能说明苯与液溴发生了取代反应的现象是_____________________。
(3)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是___________。简述这一操作的方法__________。
(4)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤、振荡、分液;②用5%的NaOH溶液洗涤、振荡、分液;③用蒸馏水洗涤、振荡、分液;④加入无水CaCl2粉末干燥;⑤_______________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是
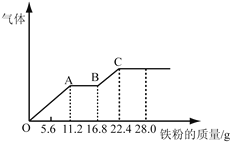
A. 混合酸中HNO3物质的量浓度为2mol/L
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 原混合酸中H2SO4物质的量为0.4 mol
D. 第二份溶液中最终溶质为FeSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com