
【题目】五氧化二钒及其他钒的化合物广泛应用于钢铁、有色合金、化工、炼油、玻璃及陶瓷等工业部门。可从含钒石煤灰渣中提钒,该试验工艺流程如下图:

表1 灰渣主要化学成分分析/%
V2O3 | SiO2 | Fe2O3 | Al2O3 | MgO | K2O | CaO | 烧失量 |
1.26 | 55.71 | 6.34 | 7.54 | 1.26 | 3.19 | 1.41 | 20.55 |
表2中间盐主要成分分析/%(以氧化物形式表示其含量)
V2O3 | Al2O3 | Fe2O3 | MgO | K2O |
5.92 | 1.70 | 18.63 | 2.11 | 3.38 |
已知:
①石煤灰渣的化学成分分析见表1,中间盐的主要成分分析见表2。
②矿物焙烧过程中,若温度过高,易发生烧结,温度越高,烧结现象越严重。
③萃取反应可以表示为:VO2++(HR2)PO4(o)→VO[R2PO4]R(o)+H+,(o)表示有机相
④有机萃取剂(HR2)PO4萃取VO2+的能力比萃取V02+要强。
请回答:
(1)提高浸取率的方法有____________,残渣的主要成分为______________________,
(2)经几级萃取后,有时候要适当加酸调整pH值,结合萃取反应方程式,说明原因_____________。反萃取操作应加入_____________试剂。
(3)中间盐溶解过程中,加铁粉的主要目的是_____________________。
(4)石煤中的钒以V(Ⅲ)为主,有部分V(Ⅳ),很少见V(Ⅴ)。如图1和如图2分别为焙烧温度和焙烧时间对钒浸出率的影响,由如图2可得最佳焙烧时间为______________h,由如图1可得最佳焙烧温度为800-850℃之间,焙烧温度在850℃以下时,钒浸出率随焙烧温度的上升几乎直线上升的原因是_________________________,当焙烧温度高超过850℃以后,再提高温度,浸出率反而下降的可能原因是:_________________________。

(5)反萃取液中的VO2+,加入氯酸钠后被氧化为VO2+,请写出该反应的离子方程式______________。然后用氨水调节pH到1.9~2.2沉钒,得多钒酸铵沉淀(化学式为(NH4)2V12O31·nH2O),再经固液分离、干燥、焙烧得五氧化二钒产品,请写出此步反应的化学方程式____________________________。
【答案】加热,提高酸的浓度,粉碎等 SiO2 随着萃取过程的进行,水相中的pH值有所下降,所以经几级萃取后需要调整pH值 H2SO4溶液 将VO2+还原为VO2+ 1.5-2.0之间 850℃以前,随着焙烧温度的升高,反应速率加快,生成的高价钒化合物更多,因此浸出率上升。 850℃以后,样品发生烧结,温度越高,烧结现象越严重,从而使钒的浸出率下降。 3H2O+6VO2++ClO3-=Cl-+6VO2++6H+ (NH4)2V12O31·nH2O![]() 6V2O5+2NH3↑+(n+1)H2O
6V2O5+2NH3↑+(n+1)H2O
【解析】
(1)结合提高产率或原料利用率的角度分析;二氧化硅不溶于硫酸;
(2)结合萃取反应分析萃取后水相的pH值变化;反萃取操作是使该萃取反应平衡向逆反应方向移动;
(3)结合已知信息④分析,铁粉具有还原性;
(4)结合图像分析作答;850℃以前,温度可影响化学反应速率和原料利用率,提高浸出率;850℃以后结合给定信息②进行解答;
(5)依据氧化还原反应的规律书写该反应的离子方程式;铵盐焙烧过程中有氨气生成,根据题意分析作答。
(1)加热,提高酸的浓度,粉碎等均可提高浸取率;加硫酸酸浸后,二氧化硅不反应,则残渣的主要成分为SiO2,
故答案为:加热,提高酸的浓度,粉碎等;SiO2;
(2)萃取反应根据VO2++(HR2)PO4(o)→VO[R2PO4]R(o)+H+可知,随着萃取过程的进行,水相中的氢离子浓度不断增大,pH值有所下降,所以经几级萃取后需要调整pH值,反萃取时,可加入适量硫酸溶液,使平衡向逆向移动,达到反萃取的目的,
故答案为:随着萃取过程的进行,水相中的pH值有所下降,所以经几级萃取后需要调整pH值 H2SO4溶液;
(3)由已知信息④可知,有机萃取剂(HR2)PO4萃取VO2+的能力比萃取VO2+要强,所以在中间盐溶液过程中,加入还原剂铁粉,可将VO2+还原为VO2+,提高原料利用率,便于后续萃取操作,
故答案为:将VO2+还原为VO2+;
(4)图2可得浸出率随着焙烧时间呈增大趋势,其最佳焙烧时间在1.5-2.0 h之间均可;浸出率随温度的变化曲线如图1,其原因是,850℃以前,随着焙烧温度的升高,反应速率加快,生成的高价钒化合物更多,因此浸出率上升;850℃以后,样品发生烧结,温度越高,烧结现象越严重,从而使钒的浸出率下降,
故答案为:1.5-2.0之间;850℃以前,随着焙烧温度的升高,反应速率加快,生成的高价钒化合物更多,因此浸出率上升;850℃以后,样品发生烧结,温度越高,烧结现象越严重,从而使钒的浸出率下降;
(5)反萃取液中的VO2+,加入氯酸钠后被氧化为VO2+,则NaClO3被还原为Cl-,根据得失电子守恒、电荷守恒、原子守恒,反应的离子方程式为6VO2++ClO3-+3H2O=6VO2++Cl-+6H+;(NH4)2V12O31·nH2O再经固液分离、干燥、焙烧得五氧化二钒产品,同时会有氨气与水生成,其化学方程式为:(NH4)2V12O31·nH2O![]() 6V2O5+2NH3↑+(n+1)H2O,
6V2O5+2NH3↑+(n+1)H2O,
故答案为:6VO2++ClO3-+3H2O=6VO2++Cl-+6H+;(NH4)2V12O31·nH2O![]() 6V2O5+2NH3↑+(n+1)H2O。
6V2O5+2NH3↑+(n+1)H2O。


科目:高中化学 来源: 题型:
【题目】如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
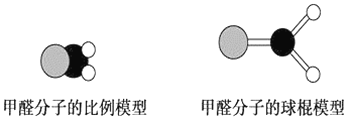
(1)甲醛分子中碳原子的杂化方式是__________,作出该判断的主要理由是__________________________。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________(填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________(填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大改变。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是____(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料红氧化铁的工艺流程如下(部分操作和条件略):
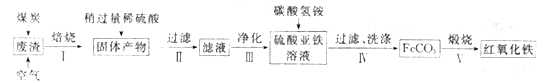
①在步骤Ⅰ中产生的有毒气体可能有_____________________。
②在步骤Ⅲ操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+ 沉淀完全,则溶液的pH为_________。(c(Al3+)≤1.0×10-5mol/L 视为Al3+沉淀完全)
③步骤Ⅳ中,生成FeCO3的离子方程式是____________________________。
(3)氯化铁溶液称为化学试剂中的“多面手”。向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生沉淀,写出该沉淀的化学式______________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:__________________________________________________________。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应Ⅱ的离子方程式是____________________________________________。
②如今基于普鲁士蓝合成原理可检测食品中是否含CN-,方案如下:

若试纸交蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是( )

A. 电极b反应式是O2+4e-+2H2O=4OH-
B. 电解后乙装置d电极附近溶液的pH不变
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 甲中每消耗1mol SO2,乙装置中有1mol H+通过隔膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为________,该元素的符号是________。
(2)Y元素原子的价层电子的电子排布图为________,该元素的名称是________。
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________。
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是___________________________________________________________。
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由
_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和食盐水,2NaCl+2H2O ![]() H2↑+Cl2↑+2NaOH 生成4mol 的NaOH,(a为饱和食盐水),下列说法正确的是
H2↑+Cl2↑+2NaOH 生成4mol 的NaOH,(a为饱和食盐水),下列说法正确的是

A. 在X极生成2mol Cl2 B. 在X极生成2molH2
C. 在Y极生成4mol Cl2 D. NaOH在Y极生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5,依次发生分解反应:①N2O5(g)![]() N2O3(g)+O2(g)、②N2O3(g)
N2O3(g)+O2(g)、②N2O3(g)![]() N2O(g)+O2(g)。在体积为2 L的恒容密闭容器中充入8 mol N2O5,加热到T ℃时反应达到平衡状态,此时O2和N2O3的物质的量分别为9 mol、3.4 mol,则T ℃时反应①的平衡常数为
N2O(g)+O2(g)。在体积为2 L的恒容密闭容器中充入8 mol N2O5,加热到T ℃时反应达到平衡状态,此时O2和N2O3的物质的量分别为9 mol、3.4 mol,则T ℃时反应①的平衡常数为
A. 10.7 B. 8.5 C. 9.6 D. 10.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PI3)引用作新敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成。回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) △H1。
CH3NH2(g)+H2O(g) △H1。
①NH3电子式为_______。
②已知该反应中相关化学键的键能数据如下:

则该反应的△H1=_______kJ·mol-1
(2)上述反应中所需的甲醇可以利用甲烷为原料在催化剂作用下直接氧化来合成。煤炭中加氢气可发生反应:C(s)+2H2(g)![]() CH4(g) △H2。在密闭容器中投入碳和H2,控制条件使其发生该反应,测得碳的平衡转化率随压强及温度的变化关系如图中曲线所示。
CH4(g) △H2。在密闭容器中投入碳和H2,控制条件使其发生该反应,测得碳的平衡转化率随压强及温度的变化关系如图中曲线所示。

①该反应的△H2_______0(填“>” 、“<”或“=”),判断理由是_______。
②在4MPa、1100K时,图中X点v正(H2)____ v逆(H2)(填“>”、“<”或“=”)。该条件下,将1molC和2molH2通入密闭容器中进行反应,平衡时测得的转化率为80%,CH4的体积分数为______。若维持容器体积不变,向其中再加入0.5mo1C和1mo1H2,再次达到平衡后,平衡常数K_____(填“增大”、“减小”或“不变”)。
③某化学兴趣小组提供下列四个条件进行上述反应,比较分析后,你选择的反应条件是______(填字母序号)。
A.5MPa 800K B.6MPa 1000K C.10MPa 1000K D.10MPa 1100K
(3)已知常温下PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3mol·L-1,Pb(NO3)2溶液与KI溶液混合可形成PbI2沉淀。现将浓度为2×10-3mol·L-1的Pb(NO3)2溶液与一定浓度的KI溶液等体积混合,则生成沉淀所需KI溶液的最小浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组运用电化学原理合成氨,其装置结构如图所示。下列有关说法不正确的是

A. 放电时,b极表面H2和CO均被氧化
B. 该电池工作时,H+由b极区迁移至a极区
C. a极的电极反应为N2+6H++6e-=2NH3
D. b极区发生反应CO+H2O=CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com