
下列有关化学用语或名称表达正确的是
A.亚硫酸的电离方程式:H2SO3 2H++SO
2H++SO
B.乙炔的分子结构模型示意图: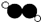
C.H2O2的电子式: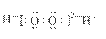
D. 的名称3-甲基-1-丁醇
的名称3-甲基-1-丁醇
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【化学—物质结构与性质】
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu的第三能层的电子排布式 ,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有 (填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为 。
(2)PO43-的空间构型是 。
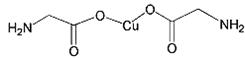
(3)氨基乙酸铜的分子结构如图,氮原子的杂化方式为 。
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,
 则CN-中含有的σ键与π键的数目之比为 。
则CN-中含有的σ键与π键的数目之比为 。
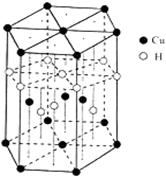
(5)Cu元素与H元素可形成一种红色化合物,其晶体结构单元
如右图所示。则该化合物的化学式为 。
(6)铜晶体为面心立方最密堆积,铜的原子半径为r pm,则晶体铜密度的计算式为 g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
C.pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中:c(NH )大小顺序:①>②>③
)大小顺序:①>②>③
D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要220mL0.5mol/L H2SO4,现用98%浓硫酸(密度为1.84g/cm3)稀释配制。
(1)本实验室中需要的仪器是 。
(2)要将浓硫酸在 中稀释,稀释时的操作方法是 。
(3)必须将稀释后的硫酸 后再移液,原因是 ,否则,所配制的稀硫酸浓度会 (偏高、偏低、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各组物质中,物质之间不可能实现如图所示转化的是

| 选项 | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是
|
c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
B.W点所表示的溶液中:
c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol·L-1
C.该温度下醋酸的电离平衡常数为10—4.75 mol·L-1
D.向X点所表示的溶液中加入等体积的0.05 mol·L-1 NaOH溶液 :
c(H+)=c(CH3COOH)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质性质的叙述中,正确的是( )
A.Cl2能与金属活动顺序表中大多数金属反应
B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2
C.硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性
D.硅是应用广泛的半导体材料,常温下化学性质活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) ⇌ 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:

下列说法不正确的是 ( )
A.该温度下此反应的平衡常数K=1.44
B.其他条件不变,升高温度,反应达到新平衡前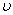 (逆)<
(逆)< 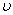 (正)
(正)
C.反应前2 min的平均速率v (Z)=4. 0×10-3mol/(L·min)
0×10-3mol/(L·min)
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com