
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | 全部 |
分析 ①先均匀加热,后局部加热可防止试管局部过热而炸裂;
②H2还原CuO时要先通H2,排净系统内的空气;
③先检查装置的气密性,否则会造成药品的浪费;
④点燃可燃性气体时要先验纯,以防发生爆炸.
解答 解:①加热试管时,先均匀加热,后局部加热可防止试管局部过热而炸裂,故①正确;
②H2还原CuO时要先通H2,排净系统内的空气,若先加热再通H2会引起爆炸,实验完毕后仍需通H2以待试管冷却,若立即停止通H2,会引起氧化,故②正确;
③制取气体物质时,要先检查装置的气密性,否则会造成药品的浪费,故③正确;
④点燃可燃性气体时要先验纯,以防发生爆炸,发生危险,故④正确;
故选D.
点评 本题考查常见仪器的使用,难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:解答题
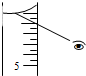 用18.4mol•L-1的浓H2SO4配制100mL浓度为1mol•L-1的稀H2SO4,其操作可分为以下各步:
用18.4mol•L-1的浓H2SO4配制100mL浓度为1mol•L-1的稀H2SO4,其操作可分为以下各步:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业可采用火法炼铜:Cu2S+O2═2Cu+SO2 每生成2mol铜,反应共转移6NA个电子 | |
| B. | 标准状况下,11.2L甲苯含有的分子数为0.5NA | |
| C. | 20g重水(D2O)所含的电子数为10NA | |
| D. | 60gSiO2中共用电子对数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
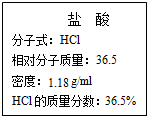 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1=V2>V3 | B. | V1=V2=V3 | C. | V3>V2>V1 | D. | V3>V2=V1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水显碱性,是因为氨水是一种弱碱 | |
| B. | 氨水和液氨成分相同 | |
| C. | 氨水中物质的量浓度最大的粒子是NH3•H2O(除水外) | |
| D. | 氨水中共有五种粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com