
【题目】对水样中M的分解速率的影响因素进行研究。 在相同温度下,M的物质的量浓度[c(M)]随时间(t)的变化如下图所示。下列说法错误的是
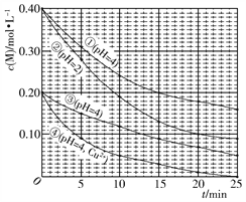
A. 水样酸性越强,M的分解速率越快
B. 水样中添加Cu2+,能加快M的分解速率
C. 由②③得,反应物浓度越大,M的分解速率越快
D. 在0~20 min内,②中M的分解速率为0.015 mol·L1·min1
【答案】C
【解析】
根据图像,A项,由①②得,c(M)起始相同时,pH越小,M的分解速率越快;B项,由③④得,在pH和c(M)起始都相同时,加入Cu2+,M的分解速率加快;C项,由①③得,pH相同时,c(M)越大,M的分解速率越快;D项,根据公式υ=![]() 计算。
计算。
根据图像,A项,由①②得,c(M)起始相同时,pH越小,M的分解速率越快,即水样酸性越强,M的分解速率越快,A项正确;B项,由③④得,在pH和c(M)起始都相同时,加入Cu2+,M的分解速率加快,B项正确;C项,②③的pH和c(M)都不相同,应由①③得,pH相同时,c(M)越大,M的分解速率越快,C项错误;D项,在0~20min内,②中M的分解速率υ=![]() =
=![]() =0.015mol/(L·min),D项正确;答案选C。
=0.015mol/(L·min),D项正确;答案选C。


科目:高中化学 来源: 题型:
【题目】(1)氮的固定是几百年来科学家一直研究的课题 。
下表列举了不冋温度下大气固氮和工业固氮的部分化学平衡常数K的值:
反应 | 大气固氮N2(g)+O2(g) | 工业固氮N2(g)+3H2 (g) | |||
温度/℃ | 27 | 2000℃ | 25 | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 200 |
①分析数据可知:大气固氮反应属于_____________ (填“吸热”或“放热”反应。
②从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因________________________________。
③在一定的温度和压强下,把2体积N2和6体积H2充入一容积可变的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。反应达到平衡后N2的质量分数为a%,若在相同容器中充入m 摩尔的N2和n 摩尔的H2也能使平衡时N2的质量分数达到a%,则m 和n 的关系用代数式表达应为___________。若在一定温度下的定容密闭容器中发生上述反应,能说明此反应已达化学平衡状态的是________。
2NH3(g) △H<0。反应达到平衡后N2的质量分数为a%,若在相同容器中充入m 摩尔的N2和n 摩尔的H2也能使平衡时N2的质量分数达到a%,则m 和n 的关系用代数式表达应为___________。若在一定温度下的定容密闭容器中发生上述反应,能说明此反应已达化学平衡状态的是________。
A.密度不变 B.混合气体平均相对分子质量不变
C.V正(N2)= 2v逆(NH3) D.N2的体积分数不再改变
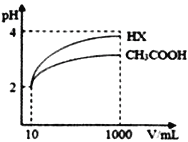
(2)体积均为10mL,pH均为2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH 变化如图:则HX 的电离平衡常数_________(填“大于”、“等于”或“小于”)醋酸的电离平衡常数。稀释后,HX溶液中水电离出来的c (H+)_______ (填“大于”、“等于”或“小于”)醋酸的溶液中水电离出来的c (H+),理由是_______________________________________。
(3)已知100℃时,水的离子积常数为1×10-12,将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表和元素周期律可指导人们进行规律性推测和判断。下列说法中不合理的是
A. 若X+和Y2﹣的核外电子层结构相同,则原子序数:X>Y
B. 硅、锗都位于金属与非金属的交界处,都可以做半导体材料
C. 盐酸(HCl)酸性比H2SiO3强,可推断出元素的非金属性:Cl>Si
D. Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.蛋白质的组成元素为碳、氢、氧、氮、硫
B.人体内油脂在小肠处水解
C.纤维素在人体内水解,为人体提供能量
D.海带提碘,灼烧时在蒸发皿中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于100mL1mol/L硫酸与铁片的反应,采取下列措施,其中能使反应速率加快的是
A. 再加入等量的铁片 B. 改用200mL 1.5mol/L盐酸
C. 改用浓硫酸 D. 升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( ) ①m+n>p
②x点表示的正反应速率大于逆反应速率
③n>p
④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大.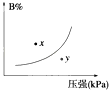
A.①②⑤
B.②④
C.①③
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一次性使用的聚苯乙烯材料带来的“白色污染”就是一种较为严重的污染现象,最近研制的一种新型材料 能代替聚苯乙烯.它是由乳酸聚合而成的.这种材料可以在乳酸菌作用下完全降解.下列关于聚乳酸的说法正确的是( ) 
A.聚乳酸是一种纯净物
B.聚乳酸的聚合方式与聚苯乙烯相似
C.聚乳酸的单体为CH3CH(OH)COOH
D.聚乳酸的链节为n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】懵圈?不是过度用脑,而是你做题太少!如下图是实验室制备SO2并验证SO2某些性质的装置图。试回答:

(1)⑥中发生的化学反应方程式为____________________________。
(2)⑤的作用是_________________,反应的离子方程式为 __________________________。
(3)②中的现象是_________________。
(4)根据③、④的现象可得出SO2具有的性质是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com