
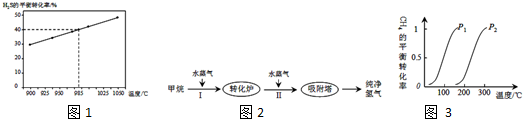
分析 (1)①根据在985℃时,H2S的转化率为40%,即可求出H2S的物质的量的该变量,然后根据在反应中,物质的量的该变量之比等于计量数之比,即可求出S2的物质的量的该变量,然后根据v=$\frac{\frac{△n}{V}}{△t}$来计算反应速率.
②据图可知,温度越高,H2S的平衡转化率越高,则说明升高温度,反应H2S=H2(g)+$\frac{1}{2}$S2(g)平衡右移,反应吸热;
(2)①采取控制变量法分析,由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动;
②依据化学平衡三段式列式计算平衡浓度结合平衡常数概念计算得到.
解答 解:(1)①985℃时,H2S的转化率为40%,H2S的物质的量的该变量△n=3.5mol×40%=1.4mol,在反应中,物质的量的该变量之比等于计量数之比,故S2的物质的量的该变量△n=0.7mol,故反应速率v(S2)=v=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.7mol}{2L}}{7min}$=0.05mol/(L•min),
故答案为:0.05 mol L-1min -1;
②据图可知,温度越高,H2S的平衡转化率越高,则说明升高温度,反应H2S=H2(g)+$\frac{1}{2}$S2(g)平衡右移,反应吸热,故反应S2(g)+2H2(g)=2H2S(g)放热,即△H<0,故答案为:<;
(2)①由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,平衡向正反应方向移动,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动,即P1<P2;故答案为:<;
②100℃时,将3mol CH4和4mol H2O通入容积为100L的恒容密闭容器中,CO(g)和H2O(g))的浓度相同,
CH4(g)+H2O(g)?CO(g)+3H2(g)
起始量(mol/L) 0.03 0.04 0 0
变化量(mol/L) 0.02 0.02 0.02 0.06
平衡量(mol/L) 0.01 0.02 0.02 0.06
平衡常数K=$\frac{c(CO)c{\;}^{3}(H{\;}_{2})}{c(CH{\;}_{4})c(H{\;}_{2}O)}$=$\frac{0.02×0.06{\;}^{3}}{0.01×0.02}$=0.0216;
故答案为:0.0216.
点评 本题综合考查化学平衡的计算,为高考常见题型和高频考点,侧重考查学生的分析、计算能力,涉及利用盖斯定律来解题和反应速率的求算、平衡的计算以及利用温度对平衡转化率的影响来分析反应吸热还是放热等,难度不大.


科目:高中化学 来源: 题型:选择题
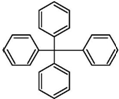 甲烷分子中的4个氢原子全部被苯基取代,所得物质的分子结构如图所示,对该物质的描述不正确的是( )
甲烷分子中的4个氢原子全部被苯基取代,所得物质的分子结构如图所示,对该物质的描述不正确的是( )| A. | 其分子式为C25H20 | |
| B. | 分子内的所有碳原子不可能共平面 | |
| C. | 该物质光照下可和氯气发生反应 | |
| D. | 该物质在Fe粉催化下可和液溴发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
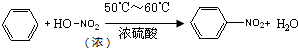
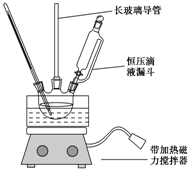 硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:
硝基苯是重要的化工原料,用途广泛.实验室用如图装置制备硝基苯,步骤如下:| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | - | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | - | 338 | 1.84 | 易溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
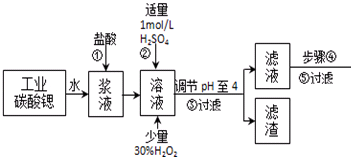
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH${\;}_{4}^{+}$、Ca2+ |
| 阴离子 | OH-、NO${\;}_{3}^{-}$、I-、HCO${\;}_{3}^{-}$、AlO${\;}_{2}^{-}$、HSO${\;}_{4}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难溶电解质Ag2SO4的饱和溶液中,若c(SO42-)=amol•L-1,则Ksp(Ag2SO4)=2a3 | |
| B. | 某氨水的pH=11,将此溶液稀释10倍后,溶液的pH<10 | |
| C. | Ka(HCN)<Ka(CH3COOH),说明相同温度下同浓度的HCN溶液的酸性比CH3COOH溶液的强 | |
| D. | pH=8的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2与CH3CH2OH均可以使KMnO4(H+)褪色,且褪色原理相同 | |
| B. | 乙酸乙酯的制取中,水浴加热的目的有:加快化学反应速率,同时使产物分离,平衡正向移动 | |
| C. | 等质量的CH3CH2OH与CH3COOH,均能与足量的金属钠发生取代反应,前者反应速率较后者慢,且生成等物质量的H2 | |
| D. | 在一溴乙烷中加入NaOH和CH3CH2OH,加热,加入HNO3酸化的AgNO3,出现淡黄色沉淀,说明溴乙烷发生了水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
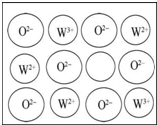 X、Y、Z、W四种元素原子序数依次增大且均小于36.Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒,W基态原子有10个价电子.回答下列问题(以下问题均以推知元素符号作答):
X、Y、Z、W四种元素原子序数依次增大且均小于36.Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒,W基态原子有10个价电子.回答下列问题(以下问题均以推知元素符号作答):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com