
| A. | 工业上炼铁的原料是赤铁矿 | |
| B. | 铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4 | |
| C. | 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入过量铁粉,然后过滤 | |
| D. | 进行焰色反应,连续做两个样品时,应将铂丝用硫酸洗净并灼烧到无特殊焰色 |
分析 A、工业上炼铁的原料是赤铁矿、焦炭;
B、铁在纯氧中燃烧生成四氧化三铁,高温下和水蒸气反应生成四氧化三铁和氢气;
C、金属铁可以和氯化铁之间反应生成氯化亚铁;
D、进行焰色反应,应将铂丝用盐酸洗净,盐酸具有挥发性.
解答 解:A、工业上炼铁的原料是赤铁矿、焦炭采用还原法进行金属铁的冶炼,故A正确;
B、铁在纯氧中燃烧生成四氧化三铁,高温下和水蒸气反应生成四氧化三铁和氢气,铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4,故B正确;
C、金属铁可以和氯化铁之间反应生成氯化亚铁,除去FeCl2溶液中的FeCl3杂质可以向溶液中加入过量铁粉,然后过滤,故C正确;
D、进行焰色反应,应将铂丝用盐酸洗净,盐酸具有挥发性,不能用硫酸来洗铂丝,故D错误.
故选D.
点评 本题考查学生元素化合物的有关知识,注意知识的归纳和梳理是关键,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
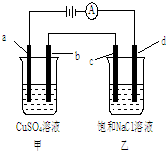
| A. | 甲烧杯中溶液的pH增大,乙烧杯中溶液的pH减小 | |
| B. | 电解一段时间后,b极质量增加,d极附近滴加酚酞溶液变红 | |
| C. | 甲烧杯中a电极发生氧化反应,电极反应式为:4OH-+4e-═O2↑+2H2O | |
| D. | C是阳极,电子从d电极通过溶液流向c电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的电极反应式为Al-3e-→Al3+ | |
| B. | 该电池的总反应式为2Li+FeS═Li2S+Fe | |
| C. | LiAl在电池中作为负极材料,该材料中Li的化合价为+1 | |
| D. | 充电时,阴极发生的电极反应式为Li2S+Fe-2e-═2Li++FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
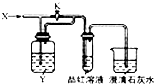 向图所示的装置中缓慢通入气体X,若打开活塞K,品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊.X和Y可能是( )
向图所示的装置中缓慢通入气体X,若打开活塞K,品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊.X和Y可能是( ) | A | B | C | D | |
| X | SO2 | Cl2 | HCl | NO2 |
| Y | NaOH溶液 | 饱和NaCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据分散质粒子能否透过滤纸,可以将分散系分为溶液、胶体和浊液 | |
| B. | 根据某物质中是否含有氢元素,判断该物质是否属于酸 | |
| C. | 根据化学反应前后,是否有电子转移,判断反应是否属于氧化还原反应 | |
| D. | 根据某物质中是否含有氧元素,可以判断该物质是否属于氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物一定是非金属氧化物,混合物、分散系、胶体有从属关系 | |
| B. | 元素的单质可由氧化或还原含该元素的化合物来制得 | |
| C. | 得电子越多的氧化剂,其氧化性就越强;含最高价元素的化合物一定具有强的氧化性 | |
| D. | 烧碱、熟石灰均属于碱,酸、碱、盐之间发生的反应均属于复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com