
科目:高中化学 来源: 题型:
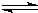 M(OH)2
M(OH)2 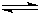 2H++MO22-
2H++MO22-查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小于10 | B、等于10 | C、大于10 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源:2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷 题型:填空题
(10分)
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:
M2+ + 2OH-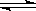 M(OH)2
M(OH)2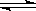 2H+ + MO22-
2H+ + MO22-
回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25Co时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-) ,C(H+) ,水的电离度 ,Kw
(2)(4分)25Co时,向A的稀溶液中加入少量的烧碱固体。
则水的电离度 ,溶液的pH
Ⅱ、.(2分)室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为 10 (填大于、等于或小于)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com