
水的电离过程为H2O H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14.则下列叙述正确的是( )
H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14.则下列叙述正确的是( )
A.c(H+)随温度的升高而降低 B.35℃时,c(H+)>c(OH-)
C.溶液:pH(35℃)>pH(25℃) D.35℃时已电离的水的浓度约为2×10-7mol/L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届河南省高三上第五次周练化学试卷(解析版) 题型:选择题
化学与生产和生活、军事、科研产品紧密相关,下列说法错误的是( )
A、家庭用的“84”消毒液与洁厕灵不能同时混合使用,否则会发生中毒事故
B、在牙膏中添入Na2PO3F、NaF能防治龋齿,当提供的F-浓度相等时,它们防治龋齿的作用是相同的
C、侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异
D、可用蘸浓盐酸的玻璃棒检验输送氨气的管道是否漏气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一下期末化学试卷(解析版) 题型:填空题
在2 L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g) △H<0,体系中,n(NO)随时间的变化如右表:
2NO2(g) △H<0,体系中,n(NO)随时间的变化如右表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)能说明该反应已经达到平衡状态的是( )
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)右图中表示NO2的变化的曲线是________,
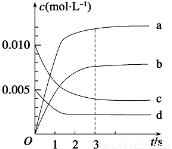
(3)用O2的浓度变化表示从0~2 s内该反应的平均速率v=____________。
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是( )
a.将容器体积变为1L b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。据图判断错误的是( )
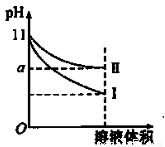
A.a的数值一定大于9
B.II为氨水稀释时溶液的pH变化曲线
C.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
D.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V( NaOH)<V(氨水)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
室温时,将xmL pH=a的稀NaOH溶液与ymL pH=b的稀盐酸充分反应.下列关于反应后溶液pH的判断,正确的是( )
A.若x=y,且a+b=14,则pH>7 B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7 D.若x=10y,且a+b=14,则pH>7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
将pH为5的盐酸溶液稀释500倍,稀释后溶液中c(Cl-)和c(H+)之比约为( )
A.1:2 B.1:5 C.1:10 D.10:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+ N(g)  E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol•L-1.下列说法正确的是( )
E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol•L-1.下列说法正确的是( )
A.4min时,M的转化率为80%
B.4min时,用M表示的反应速率为0.8mol•L-1•min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.2min时,M的物质的量浓度为0.6mol•L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列叙述正确的是( )
A.在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA
B.常温常压下,16gO3所含的电子数为8NA
C.5NH4NO3  2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
D.铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:填空题
(1)下图是某煤化工产业链的一部分,已知该产业链中某反应的平衡常数表达式为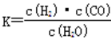 ,已知此反应中生成1g氢气需吸热65.75kJ,它所对应的热化学方程式是 。
,已知此反应中生成1g氢气需吸热65.75kJ,它所对应的热化学方程式是 。

(2)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是 (填“低温”、“高温”或“任意温度”)
②下列叙述能说明容器内反应达到平衡状态的是 。
A.混合气体的平均相对分子质量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变
(3)改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0中的所有物质都为气态,起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态,起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
反应I恒温恒容 | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 | ||||
反应II绝热恒容 | 0min | 0 | 0 | 2 | 2 |
到平衡时,反应I、II对比,平衡时CH3OH的浓度c(I) c(II)(填“>”“<”或“=”)
反应I,前10min内的平均反应速率v(CH3OH)= 。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡 移动。(填“正向”“逆向”或“不”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com