
���п�ͼ�е����ʾ�Ϊ��ѧ��ѧ�г������ʣ����мס���Ϊ���ʣ������Ϊ�����BΪ����Һ̬�����AΪ����ɫ���壬F��G����Ԫ����ͬ�Ҿ�Ϊ�Ȼ��G��KSCN��Һ�Ժ�ɫ��
��ش��������⣺
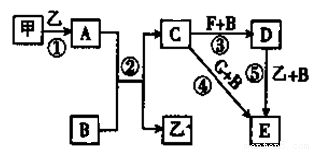
��1��A�� ��G��
��2����Ӧ��~���У�����������ԭ��Ӧ���� ������ţ���
��3����Ӧ�ݵĻ�ѧ����ʽΪ ������B��Ӧ�����ӷ���ʽΪ ��
���ڿ����н�C��Һ����F��Һ�У��۲쵽�������� ��
 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016����������ɽ����ѧ�����ϵڶ����¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
[��ѧѡ��2������ѧ�뼼��]��15�֣�
��Ϣʱ�������Ĵ������������Ի��������˼������в��ij�����Ϊ����ѧ��̽��С�飬��һ����������·�������õ���70%Cu��25%Al��4%Fe������Au��Pt�Ƚ����Ļ�������������Ʊ�����ͭ�������������·�ߣ�
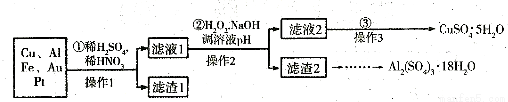
��ش��������⣺
��1���ڢٲ�Cu���ᷴӦ�����е����ӷ���ʽΪ_______���õ�����1����Ҫ�ɷ�Ϊ___________��
��2���ڢڲ���H2O2��������___________��ʹ��H2O2���ŵ���___________������ҺpH��Ŀ����ʹ________________���ɳ�����
��3���õڢ۲�����CuSO4��5H2O�Ʊ���ˮCuSO4�ķ�����_______________________��
��4��������2��ȡAl2��S04��3•18H2O��̽��С����������ַ�����
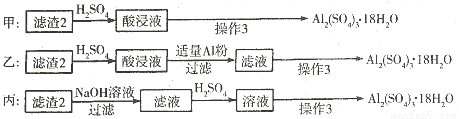
�������ַ����У�________���������У�ԭ����________________��ԭ�������ʽǶȿ��ǣ�__________������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶��϶������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���1.000mol•L-1�������20.00mL 1.000mol•L-1��ˮ�У���ҺpH���¶��������������仯������ͼ��ʾ�������й�˵����ȷ���ǣ� ��
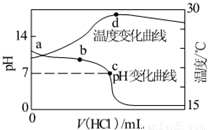
A��a����ˮ�������c��H+��=1.0��10-14mol•L-1
B��b�㣺c��NH4+��+c��NH3•H2O��=c��Cl-��
C��c�㣺c��Cl-��=c��NH4+��
D��d��������¶����½�����Ҫԭ����NH3•H2O��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��϶����¿���ѧ�Ծ��������棩 ���ͣ������
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ҵ�Ϻϳɰ���Ӧͨ��������ý����������Ӧ����ʽΪ��N2+3H2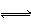 2NH3 ��H<0��
2NH3 ��H<0��
��1����֪N2(g)+3H2(g) 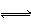 2NH3(g) ��H����92kJ��mol��1 ����1mol H��H����1molN��N���ֱ���Ҫ��������436kJ����946kJ�����1molN��H����Ҫ��������__________��
2NH3(g) ��H����92kJ��mol��1 ����1mol H��H����1molN��N���ֱ���Ҫ��������436kJ����946kJ�����1molN��H����Ҫ��������__________��
��2���ϳɰ���Ӧ�ﵽƽ����������ݻ�ѹ����ԭ����1/2�������������䣬��ƽ����ϵ������Ӱ���� ������ĸ��ţ���
A��c(H2)��С B������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
C��NH3�����ʵ������� D��ƽ�ⳣ��K����
E.ƽ�����������ƶ�
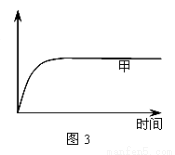
��3�� ��ͼ2��ʾ���ڼס����������зֱ����1molN2��3molH2��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����ӦN2(g)+3H2(g) 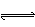 2NH3(g) ����ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������H2��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������H2��ת������ʱ��仯��ͼ��
2NH3(g) ����ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������H2��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������H2��ת������ʱ��仯��ͼ��
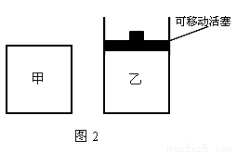
��4������ӦN2(g)+3H2(g) 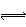 2NH3(g)��һ�ݻ��̶�����������ڽ��У���ά�ַ�Ӧ�������¶Ȳ��䡣��ƽ���������������ʼʱN2��H2�����ʵ����ֱ�Ϊamol��bmol����a:b=______ʱ���ﵽƽ���NH3������������
2NH3(g)��һ�ݻ��̶�����������ڽ��У���ά�ַ�Ӧ�������¶Ȳ��䡣��ƽ���������������ʼʱN2��H2�����ʵ����ֱ�Ϊamol��bmol����a:b=______ʱ���ﵽƽ���NH3������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����±�������ѡ���д������
��ѧʽ | NH3��H2O | CH3COOH | HCN | H2CO3 |
����ƽ�ⳣ����25�棩 | 1.8��l0��5 | 1.8��l0��5 | 4.9��l0��10 | K1= 4.3��l0��7�� K2= 5.6��l0��11 |
A��0.1mol��L��1 CH3COONa ��Һ�Լ��ԣ�0.1mol��L��1 CH3COONH4 ��Һ������
B�������ʵ���Ũ�ȵ�NaHCO3��NaCN��Һ��ǰ����Һ��ˮ�ĵ���̶ȴ�
C��NaCN + H2O + CO2 (����) = HCN + NaHCO3
D������3�ֵ������pH������Һ���ֱ��ˮϡ�ͺ�pH����ȣ�������м���ˮ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ������
��1����ͼ��ʾ��A�Ǻ��ݵ��ܱ�������B��һ������ɱ�ij������ҡ����ֺ��£��ر�K2����1molN2��3molH2ͨ��K3����B�У���2molN2��6molH2ͨ��K1����A�У���ʼʱA��B�������ͬ��ΪaL���ﵽƽ��ʱ��V(B)=0.8aL��
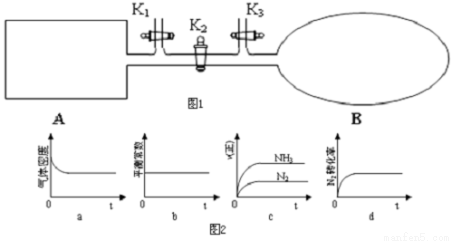
��ͼ2ʾ��ͼ����ȷ���Ҽ���˵��A�����з�Ӧ�ﵽƽ��״̬������˵��B�����з�Ӧ�ﵽƽ��״̬����______��
��A��B��N2ת���ʵĹ�ϵ����(A) ___��(B)���>������<����������
�۴�K2��һ��ʱ���ִﵽƽ��ʱ��B�����Ϊ_____L����ͨ��������������ƣ�
��2��ij�о�С���һԪ�л�����HA���ܼ�����ˮ�Ļ����ϵ���ܽ�̶Ƚ����о�����25��ʱ������HA��ˮ�в��ֵ��룬��HAŨ��Ϊ4.0��10-3mol•L-1ʱ��������Ϊ0.30���ڱ��в��ַ���˫�ۣ����ɣ�HA��2����ƽ����ϵ�У�һԪ�л�����HA���ܼ�����B����ˮ��W���еķ���ϵ��ΪK��K=c(HA)B/c(HA)W=1.0�����ﵽƽ����Է�����ʽ���ڵ�HA�ڱ���ˮ�����ܼ��еı���Ϊ1��1��������Ϣ���£�
25��ƽ����ϵ | HA��ʼ��Ũ�� |
��ˮ�У�HA | 4.0��10-3mol•L-1 |
�ڱ��У�2HA | 5.0��10-3mol•L-1 |
��25�棬�ڱ���ϵ��HA��ת����Ϊ___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
a mol FeS��b mol FeOͶ�뵽v L��c mol•L��1��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ijɷֿɿ�����Fe(NO3)3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
��(a+b)��63g ��(a+b)��189g ��(a+b)mol ��[cV��(9a+b)/3 ]mol
A���٢� B���ڢ� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��������Ϫ��һ��ѧ������ѧ�����п�������ѧ�Ծ��������棩 ���ͣ�ʵ����
�ߴ�MnCO3���Ʊ������ܴ��Բ��ϵ���Ҫԭ�ϡ�ʵ������MnO2Ϊԭ���Ʊ������ߴ�MnCO3�IJ����������£�
��1���Ʊ�MnSO4��Һ������ƿ�У�װ�ü���ͼ������һ����MnO2��ˮ�����裬ͨ��SO2��N2������壬��Ӧ3h��ֹͣͨ��SO2��������ӦƬ�̣�����.
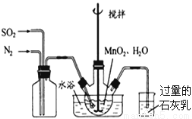
�� д�������ƿ������ ��
�� ʯ�����������: ���û�ѧ����ʽ��ʾ��
�� д��MnO2��H2SO3��Ӧ�����ӷ�Ӧ����ʽ ��
�ܷ�Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ�� (ѡ��ѡ�����)��
a������ͨ�������� b������ͨ��������c�������ʵ����¶� d�����¼���
��2���Ʊ��ߴ�MnCO3���壺��֪MnCO3������ˮ���Ҵ�����ʪʱ�ױ����������� 100�濪ʼ�ֽ⣻Mn(OH)2��ʼ����ʱpH=7.7���벹���ɣ�1���Ƶõ�MnSO4�Ʊ��ߴ�MnCO3�IJ������衾ʵ���п�ѡ�õ��Լ��� Ca(OH)2��NaHCO3��Na2CO3��C2H5OH����
100�濪ʼ�ֽ⣻Mn(OH)2��ʼ����ʱpH=7.7���벹���ɣ�1���Ƶõ�MnSO4�Ʊ��ߴ�MnCO3�IJ������衾ʵ���п�ѡ�õ��Լ��� Ca(OH)2��NaHCO3��Na2CO3��C2H5OH����
�� �߽������Na2CO3����������ҺpH��7.7��
�� ��
�� ����SO42-�Ƿ�ϴ�Ӹɾ�������ˮϴ�Ƿ�ϸ�ķ����� ��
�� ������C2H5OHϴ�ӣ���Ŀ���� ��
�� ����1 00����
00����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ��12�µ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�л���ķ���ʽΪC9H18O2�������������¼�ˮ��Ϊ�Һͱ������л������ͬ���¶Ⱥ�ѹǿ�£�ͬ�������Һͱ���������ռ�����ͬ����Ŀ��ܽṹ�� ( )
A��8�� B��14�� C��16�� D .18��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com