
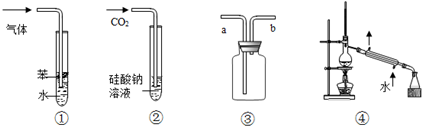
| A. | 装置①:可用于吸收NH3或HCl气体,并防止倒吸 | |
| B. | 装置②:持续通入CO2气体,先出现白色沉淀,后变澄清 | |
| C. | 装置③:若“a进b出”可用于收集NO2,若“b进a出”可用于收集NH3 | |
| D. | 装置④:可用于分离石油,得到汽油、煤油和柴油等各种纯净物 |
分析 A.苯在上层,不能隔绝气体与水;
B.反应生成硅酸沉淀;
C.密度比空气密度大的气体从a进入,收集密度比空气密度小的气体从b进入;
D.分馏产品为混合物.
解答 解:A.苯在上层,不能隔绝气体与水,则不能防止倒吸,故A错误;
B.反应生成硅酸沉淀,沉淀不能消失,故B错误;
C.密度比空气密度大的气体从a进入,收集密度比空气密度小的气体从b进入,则若“a进b出”可用于收集NO2,若“b进a出”可用于收集NH3,故C正确;
D.分馏产品为混合物,则用于分离石油,得到汽油、煤油和柴油等各种混合物,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验装置的作用、混合物分离方法等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1L C2H5OH完全燃烧后生成的CO2分子个数约为NA/11.2 | |
| B. | 将lmol Cl2通人水中,HClO、Cl一、ClO-粒子数之和为2NA | |
| C. | 含3.0g HCHO的水溶液中原子总数为0.4 NA | |
| D. | 3.4gNH3中共用电子对数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用活性炭吸附新装修居室里的有害气体 | |
| B. | 用K2Cr2O7检查司机是否酒后驾车 | |
| C. | 用盐酸清洗陶瓷面盆上的铁锈迹 | |
| D. | 用石灰水吸收燃煤烟气中的SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化、煤的液化和煤的干馏均属于化学变化 | |
| B. | 淀粉、纤维素、油脂、蛋白质均属于高分子化合物 | |
| C. | 棉花、羊毛和蚕丝都属于天然高分子 | |
| D. | 陶瓷、水泥和玻璃均属于硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
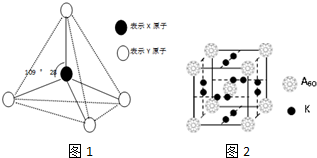
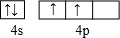 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:HBr>HI | |
| B. | 0.1 mol•L-1溶液的pH:NaOH>LiOH | |
| C. | 向Na2SO3溶液中加盐酸,有气泡产生 | |
| D. | Mg、Al与同浓度盐酸反应,Mg更剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与Z同族的第五周期元素的原子序数为50 | |
| B. | Y的简单氢化物的沸点和热稳定性均大于R的简单氢化物 | |
| C. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2,且均能与水反应 | |
| D. | 由W和Z组成的ZW物质硬度大、熔沸点高,具有导磁性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com