
| 选项 | 实验试剂 | 现象 | 解释 | 实验操作 |
| A | 试剂1:5%的H2O2溶液 试剂2:酸性KI淀粉溶液 | 溶液变蓝 | I--被H2O2氧化成I2,I2遇淀粉变蓝 |  |
| B | 试剂1:SO2的水溶液 试剂2:滴有酚酞的NaOH溶液 | 溶液褪色 | SO2具有漂白性,将酚酞漂白 | |
| C | 试剂1:乙醇 试剂2:酸性KMnO4溶液 | 溶液褪色 | 乙醇将KMnO4还原,自身被氧化为乙醛 | |
| D | 试剂1:FeCl3溶液 试剂2:待检溶液 | 溶液变红 | 待检溶液中含有SCN-,与Fe3+反应生成红色的[Fe(SCN)6]4- |


科目:高中化学 来源: 题型:
 实验室合成乙酸乙酯粗产品的步骤如下:
实验室合成乙酸乙酯粗产品的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素A、C、D的单质均能与E的单质反应,且反应均为放热反应 |
| B、元素D的最高价氧化物与B、C、E的最高价氧化物对应的水化物之间均能发生反应 |
| C、化合物AE与CE含有相同类型的化学键 |
| D、元素B、D分别与E形成的化合物中每个原子最外层均满足8电子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有100mL NaOH溶液,现向其中逐渐通入一定量的CO2,随后向此溶液中逐滴加入4mol/L的盐酸溶液,产生的CO2气体体积(标准状况下)与所加入盐酸溶液的体积之间的关系如图所示,试求:
有100mL NaOH溶液,现向其中逐渐通入一定量的CO2,随后向此溶液中逐滴加入4mol/L的盐酸溶液,产生的CO2气体体积(标准状况下)与所加入盐酸溶液的体积之间的关系如图所示,试求:查看答案和解析>>
科目:高中化学 来源: 题型:
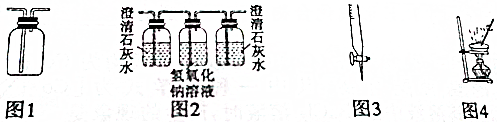
| A、用图1所示装置可以收集H2、NH3、CO2、NO2等气体 |
| B、用图2所示装置可以验证SO2气体中含有CO2气体 |
| C、用图3所示仪器可以量取Na2CO3溶液 |
| D、用图4所示装置可以进行硫酸铜晶体中结晶水含量的测定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (提示:环丁烷
(提示:环丁烷 可简写成
可简写成 )
)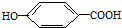 ),其反应类型
),其反应类型查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B、在能与Si反应产生H2的溶液中:NH4+、K+、SO32-、NO3- |
| C、在能与Al反应产生H2的溶液中:NH4+、Al3+、SO42-、NO3- |
| D、在pH=1的溶液中:K+、Fe3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO3 |
| B、SO42- |
| C、NH4+ |
| D、Br |
查看答案和解析>>
科目:高中化学 来源: 题型:
 金属铁及其化合物在合金材料以及催化剂等方面应用广泛.请回答下列问题:
金属铁及其化合物在合金材料以及催化剂等方面应用广泛.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com