
【题目】表示下列反应的离子方程式正确的是
A. 在强碱性溶液中次氯酸钠与 Fe(OH)3 反应生成 Na2FeO4: 3ClO3-+2Fe(OH)3 =2FeO42-+3Cl-+H2 O+4H+
B. 用浓盐酸与 MnO2 反应制取少量氯气:MnO2+2H++2Cl-= Mn2++Cl2↑+2H2O
C. 向 NaAlO2 溶液中通入过量 CO2 制 Al(OH)3:AlO2-+CO2+2H2O===Al(OH)3↓+HCO3-
D. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-===3Fe3++NO2↑+3H2O
【答案】C
【解析】
A.在强碱溶液中NaClO与Fe(OH)3发生氧化还原反应生成Na2FeO4、氯化钠和水,离子方程式为3ClO-+4OH-+2Fe(OH)3=3Cl-+5H2O+2FeO42-,故A错误;
B.氢原子不守恒,浓盐酸与MnO2反应的离子方程式为MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O,故B错误;
Mn2++Cl2↑+2H2O,故B错误;
C.NaAlO2溶液与过量的CO2反应的离子方程式为:AlO2-+CO2+2H2O===Al(OH)3↓+HCO3-,故C正确;
D.磁性氧化铁是Fe3O4,Fe3O4不溶于水,不能拆写,离子方程式为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故D错误。
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.液氨用作制冷剂发生的是化学反应
B.氨气溶水得到氨水发生的只是物理变化
C.分离液态空气制取氮气属于氮的固定
D.氮气与氢气化合生成氨气属于人工固氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的VL密闭容器中充入4molNH3和5molO2,发生如下反应:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g)。请回答下列问题:
4NO(g)+6H2O(g)。请回答下列问题:
(1)下列能说明该反应已经达到平衡状态的是_______;
A 容器中气体总质量不变
B c(O2)不变
C v(O2)=1.25v(NH3)
D 体系压强不变
E 相同时间内,消耗0.1 mol NH3,同时消耗了0.1 mol NO
(2)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小。则速率逐渐增大是因为______,速率又逐渐减小的原因是_____。
(3)1mol NH3(g)在纯氧中完全燃烧生成无污染的气态物质,放出akJ的热量。写出该反应的热化学方程式__________________________________________。
(4)若将(3)所述反应设计为电解质溶液为KOH的原电池,则负极反应式 _________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图提供的信息,下列所得结论不正确的是
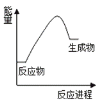
A. 该反应是吸热反应
B. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才能发生
C. 该反应反应物断裂旧键所吸收的能量高于生成物形成新键放出的能量
D. 该反应可能是碳酸钙分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 X、Y、Z、W的原子序数依次增大, X的原子在周期表中半径最小,Y的次外层电子数是其最外层的![]() ,Z单质可与冷水缓慢反应产生X单质,W与 Y属于同一主族。下列叙述正确的是( )
,Z单质可与冷水缓慢反应产生X单质,W与 Y属于同一主族。下列叙述正确的是( )
A. 由Y元素形成的离子与 Z元素形成的离子的核外电子总数可能相同
B. 单质的氧化性:W>Y
C. 化合物X2Y、ZY、ZX2 中化学键的类型均相同
D. 原子半径:rw>rz>rY
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) + O2(g) ![]() 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
甲 | 乙 | 丙 | ||
起始物质的量 | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2的平衡转化率 / % | 80 | α1 | α2 | |
A. 甲中反应的平衡常数小于乙
B. 平衡时,丙中c(SO3)是甲中的2倍
C. 该温度下,平衡常数值为400
D. 平衡时,甲中O2的转化率大于乙中O2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.离子化合物中可能含有共价键
B.分子晶体中的分子内不含有共价键
C.分子晶体中一定有非极性共价键
D.分子晶体中分子一定紧密堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1 mol石墨转变成金刚石需要吸收1.9 kJ的热量该反应的热化学方程式是__________。
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_________。
(3)已知下列热化学方程式
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
写出FeO(s)被CO还原成Fe和CO2的热化学方程式_________________。
(4)向足量H2SO4溶液中加入100 mL 0.4 mol·L-1Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com