
分析 (1)计算元素质量分数,结合n=$\frac{m}{M}$计算C、H、O原子数目之比,进而确定最简式,可得最简式的式量;
(2)结合消耗氢氧化钠计算A的物质的量,根据M=$\frac{m}{n}$计算相对分子质量,结合最简式确定分子式.
解答 解:(1)分子中C、H、O原子数目之比=$\frac{40%}{12}$:$\frac{6.67%}{1}$:$\frac{1-40%-6.67%}{16}$=1:2:1,故A的最简式为:CH2O,最简式的式量为12+2+16=30
故答案为:CH2O;30;
(2)A是一元羧酸,0.60g A消耗0.01mol NaOH,则A的物质的量为0.01mol,故A的相对分子质量为$\frac{0.6}{0.01}$=60,A的最简式为CH2O,则A的分子式为C2H4O2,
故答案为:60;C2H4O2.
点评 本题考查有机物分子式确定,熟练掌握官能团的性质与转化,掌握燃烧法利用原子守恒确定有机物分子式.


科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| B. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| C. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位 | |
| B. | 硅的化学性质不活泼,在常温下不与任何物质反应 | |
| C. | 硅在电子工业中是最重要的半导体材料 | |
| D. | 硅的性质很稳定,能以单质的形式存在于自然界中 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:R<Z<Y | B. | 简单氢化物的热稳定性:R>Y | ||
| C. | R与Y只能形成一种化合物 | D. | 最高价氧化物的水化物酸性:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
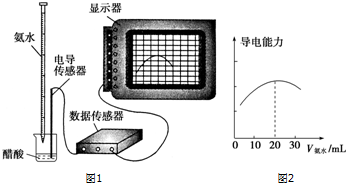
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
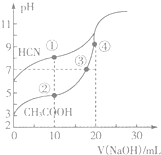 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,滴定曲线如图所示.下列说法不正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,滴定曲线如图所示.下列说法不正确的是( )| A. | 点①溶液的c(CN-)<点②溶液的c(CH3COO-) | |
| B. | 点②溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 点③溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 点④溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.5g | B. | 10.5g | C. | 13.2g | D. | 24.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32gO2和O3的混合气体所含原子数为2NA | |
| B. | 0.5mol/L MgCl2溶液中,含有Cl-离子数为NA | |
| C. | 2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA | |
| D. | 1mol碳正离子(CH 3+)所含的电子总数为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应是个放热反应 | |
| B. | 反应物的总能量高于生成物的总能量 | |
| C. | H2O2仅为氧化剂 | |
| D. | H2O2既是氧化剂又是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com