
A、
| ||
B、
| ||
C、
| ||
D、
|
| V |
| Vm |
| n |
| V |
| aL |
| 22.4L/mol |
| a |
| 22.4 |
| a |
| 22.4 |
| 36.5a |
| 22.4 |
| 36.5a |
| 22.4 |
| 36.5a |
| 22.4 |
(1000+
| ||
| 1000bg/L |
| 22400+36.5a |
| 22400b |
| ||
|
| 1000ab |
| 22400+36.5a |


科目:高中化学 来源: 题型:

 (B2H6为乙硼烷)
(B2H6为乙硼烷)查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 四 | ? | ? | ? | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、其它条件不变,加入催化剂,△H变大 |
| B、及时除去二氧化碳,正反应速率加快 |
| C、降低温度,可提高反应物的转化率 |
| D、若气体的密度保持不变,说明平衡不发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化还原反应的本质是化合价发生变化 |
| B、有单质产生的分解反应一定是氧化还原反应 |
| C、在同一氧化还原反应中,反应物和生成物中都有氧化剂 |
| D、还原剂在反应中失去电子发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向次氯酸钙溶液通入少量CO2:2ClO-+H2O+CO2=CO32-+2HClO |
| B、向明矾溶液中加入足量Ba(OH)2溶液:Al3++2SO42-+4OH-+2Ba2+=2BaSO4↓+[Al(OH)4]- |
| C、向FeCl3溶液中加入足量单质锌:Zn+2Fe3+=Zn2++2Fe2+ |
| D、向NaHSO4中滴加Ba(OH)2溶液至中性:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠熔化成银白色小球 |
| B、在液面快速游动 |
| C、溶液底部出现光亮的银白色固体 |
| D、溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
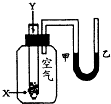 某学生用如右图所示的装置进行化学反应X+2Y→2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到试管中甲处液面下降,乙处液面上升.关于该反应的下列叙述正确的是( )
某学生用如右图所示的装置进行化学反应X+2Y→2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到试管中甲处液面下降,乙处液面上升.关于该反应的下列叙述正确的是( )| A、①②③ | B、①③ | C、②③ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,烧杯中都盛有稀硫酸:
如图所示,烧杯中都盛有稀硫酸:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com