
| A.Na2O2用作呼吸面具的供氧剂 |
| B.NaHCO3的热稳定性大于Na2CO3 |
| C.乙醇可与金属钠反应放出氢气 |
| D.金属钠着火时,可用细沙覆盖灭火 |
科目:高中化学 来源:不详 题型:单选题
| A.将钠投入足量的水中 |
| B.将钠用耐热塑料薄膜包好并刺一些小孔,再放入足量的水中 |
| C.将钠投入足量的稀硫酸中 |
| D.将钠用铝箔包好并刺一些小孔,再放入足量的水中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
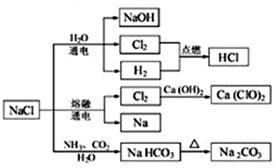
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.如图所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
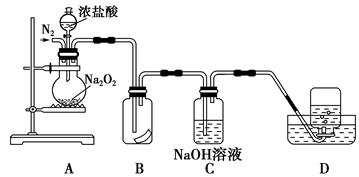
 Na2O2+
Na2O2+ HCl=
HCl= Cl2+
Cl2+ NaCl+
NaCl+ 该反应 (填“能”或“不能”)用于实验室快速制取纯净的Cl2,理由是 (要求答出两点)。
该反应 (填“能”或“不能”)用于实验室快速制取纯净的Cl2,理由是 (要求答出两点)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
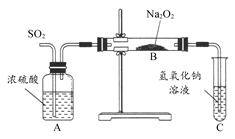
| A.①中反应,过氧化钠作氧化剂,水作还原剂 |
| B.②中反应既是化合反应又是放热反应 |
| C.③中的实验现象证明溶液中不含有Fe2+ |
| D.将①中所得溶液加入到③的溶液中,静置,溶液颜色加深 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
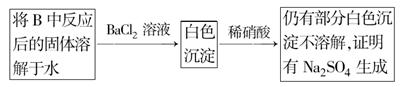
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过氧化钠和水反应生成氢氧化钠和氧气 |
| B.过氧化钠和水反应的产物是过氧化氢和氧气 |
| C.过氧化氢在二氧化锰催化作用下分解生成氧气和水 |
| D.过氧化钠跟水反应生成氢氧化钠和过氧化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:NaHCO3<Na2CO3 |
| B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3 |
| C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3 |
| D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com