
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A.实验室用H2O2分解制O2,加入MnO2作催化剂后,反应速率明显加快
B.2SO2+O2![]() 2SO3反应中,SO2的转化率能达到100%
2SO3反应中,SO2的转化率能达到100%
C.日常生活中用冰箱冷藏食物可降低食物变质的反应速率
D.可逆反应在一定条件下达到化学反应限度时正反应速率和逆反应速率相等
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是
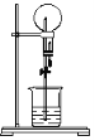
A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
D.HCl、NH3和SO2均能用该装置做喷泉实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 甲酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O
B. 醋酸溶液与Cu(OH)2:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液通少量CO2 :2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 甲醛溶液与足量的银氨溶液共热:HCHO +4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓ +6NH3+2H2O
CO32-+2NH4++4Ag↓ +6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是一种重要的化工原料。请回答下列问题。
⑴请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
![]()
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和__________________。
②在蒸发过程中,待________时,停止加热,利用余热将滤液蒸干。
⑵由于粗盐中含有MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如下图。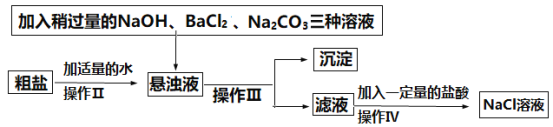
除杂质过程中用到下列操作: a.加入适量稀盐酸 b.加入过量BaCl2溶液 c.加入过量Na2CO3溶液 d.加入过量NaOH溶液
①除去可溶性杂质加入试剂的正确顺序是_____________(填序号)
②证明SO42-已经沉淀完全的方法是__________。
③加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是_____(用化学方程式表示)。
④操作Ⅳ所得滤液中加入一定量的盐酸,用玻璃棒搅拌直到没有气泡冒出,还要进行____(操作)。然后将滤液倒入蒸发皿蒸发。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于图示四个装置的叙述不正确的是( )

A. 装置甲的a端产生的气体能使湿润的淀粉碘化钾试纸变蓝
B. 装置乙可用于测定化学反应的反应热
C. 装置丙是可以在铁钉上镀铜的装置
D. 装置丁若为电解精炼铜装置,则X电极为精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B. MgCl2(aq)![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgO (s)
MgO (s)
C. S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
D. N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将35g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2L(标准状况),其质量为19.6g,则剩余锌粉的质量为
A. 1.0g B. 2.0g C. 2.5g D. 3.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) △H1=-112.3kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) △H2=-234kJ·mol-1
③N2(g)+O2(g)=2NO(g) △H3=+179.5kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式___。
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。

①b点时,平衡体系中C、N原子个数之比接近___;
②a、b、c三点CO的转化率从大到小的顺序为___;a、c、d三点的平衡常数从大到小的顺序为___。
③若n(CO)/n(NO)=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为__。
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极处通入的气体为____(填化学式);A电极的电极反应式为____;一段时间后,若乙中需加0.2molCu(OH)2使溶液复原,则转移的电子数为___。
(4)已知:25℃时,H2C2O4的电离常数Ka1=5.9×10—2,Ka2=6.4×10-5,则25℃时,0.1mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为____,若向该溶液中加入一定量NaOH固体,使c(HC2O4-)=c(C2O42-),则此时溶液呈___(填“酸性”“碱性”或“中性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com