
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:读想用 高二化学(上) 题型:038
某工厂用氨氧化法可制得质量分数为20%的硝酸,脱水后可进一步得到质量分数为90%的硝酸.若以17 t液氨为原料生产硝酸(假设反应及脱水过程中各反应物和生成物均无损耗)试回答下列问题.
(1)若该工厂同时生产质量分数分别为50%和90%的硝酸,它们的质量比为x=m1/m2(m1、m2分别为质量分数为50%的HNO3和90%的硝酸的质量).
①写出理论所需水量y与质量比x的函数关系式.
②当进出水量保持平衡时,x是多少,此时两种产品的总质量为多少吨.写出计算过程.
(2)若该工厂只生产质量分数为90%的HNO3,计算理论上需水的质量.
(3)若该工厂只生产质量分数为50%的HNO3,计算理论上需水的质量.
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
 CO2(g) +H2(g) △H=-42KJ/mol
CO2(g) +H2(g) △H=-42KJ/mol 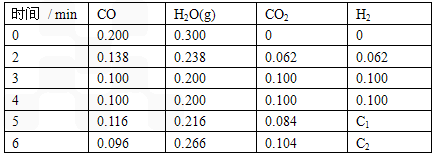
查看答案和解析>>
科目:高中化学 来源: 题型:
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D是中学化学常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱。写出A与强碱溶液反应的离子方程式: 。
(2)B、D都是酸性氧化物,且组成元素相同。B、D分子中除氧外所含另一种元素在两种化合物中的质量分数分别为50%和40%,则B、D分子中除氧外所含另一种元素在周期表中的位置为 。
 (3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式是
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式是
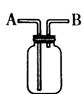
。制得的气体可用如图所示装置收集,则
气体应从 (填“A”或“B”)通入。E中所含化学键类型为
。(填“极性键”或“非极性键”)
(4)单质F的电子式为 。由各分解产物的物质的量之比推测X的组成类似于明矾,则X化学式为 。
(5)取一定量的X晶体分解,若生成F 1mol,则必同时生成 物质 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com