
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下。
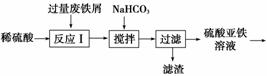

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH,使溶液中的________沉淀,该工艺中“搅拌”的作用是__________。
(2)在实际生产中,反应Ⅱ中常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作________。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________.
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+可部分水解生成聚合离子Fe2(OH) 。该水解反应的离子方程式为__________________。
。该水解反应的离子方程式为__________________。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO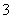 。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母序号)。
。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母序号)。
A.氯水 B.KSCN溶液
C.NaOH溶液 D.酸性KMnO4溶液
答案 (1)Al3+ 加快反应速率
(2)氧化剂 2 mol
(3)2Fe(OH)2++2H2OFe2(OH) +2H+
+2H+
(4)D
解析 (1)废铁屑中含有氧化铝,反应Ⅰ中引入了杂质Al3+,加入NaHCO3调节pH至4.4可使Al3+完全沉淀。“搅拌”的目的是使反应物充分接触,从而加快化学反应速率。(2)硫酸亚铁溶液中加入NaNO2得到Fe(OH)SO4,铁的化合价升高而N的化合价降低,故NaNO2在反应中作氧化剂。1 mol O2可得到4 mol电子,1 mol NaNO2可得到1 mol电子,标况下11.2 L O2的得电子能力与2 mol NaNO2相当。(4)Fe2+能使酸性高锰酸钾溶液褪色,故可用酸性KMnO4溶液检验产品中是否含有Fe2+。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.含有羟基的化合物一定属于醇类
B.代表醇类的官能团是跟链烃基相连的羟基
C.醇类和酚类具有相同的官能团,因而具有相同的化学性质
D.分子内有苯环和羟基的化合物一定是酚类
查看答案和解析>>
科目:高中化学 来源: 题型:
铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
A.Fe(OH)3 Fe2O3 B.Fe(OH)2 Fe2O3
C.Fe(OH)2 Fe(OH)3 D.Fe(OH)2 Fe3O4
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟 工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
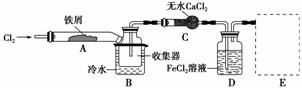
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用 干燥的N2赶尽Cl2,将收集器密封。
干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为_______________________________________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是__________________________________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)____________。
(4)装置B中冷水浴的作用为______________________________________________;
装置C的名称为________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:_________________________________________。
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)FeCl3与H2S反应的离子方程式为_________________________________________
________________________________________________________________________。
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为____________________。
(8)综合分析实验 Ⅱ 的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;
②_________________________________________________ _______________________。
_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是 ( )
A.白色沉淀是BaSO4和BaSO3
B.溶液的酸性增强
C.白色沉淀是BaSO4
D.FeCl3全部被还原为FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.10 mol·L—1CH3COOH溶液中存在如下电离平衡:
CH3COOH  CH3COO— +H+ 对于该平衡,下列叙述正确的是:
CH3COO— +H+ 对于该平衡,下列叙述正确的是:
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.10 mol·L—1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素A、B、C、D ,它们原子的电子层数与最外层电子数之比分别是1∶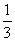 ,1∶1 ,1∶2和1∶3 。
,1∶1 ,1∶2和1∶3 。
据此回答下列问题:
(1)仅根据上述信息就能够确定的元素是 (选填A、B、C、D)。
(2)在所有满足上述信息的短周期元素中,最高价氧化物的水化物酸性最强的是(填化学式) ;由A、D两元素构成的化合物A2D2的电子式为(用元素符号填写,下同) 。
(3)在满足上述信息的短周期元素中,若B2、CD和由B、C、D形成的化合物X的混合物m g ,在一定条件下与过量氧气反应后,将产物通过足量的固体A2D2 ,最终发现固体质量增重为m g ,则符合此条件的X的分子组成可用通式( )x·( )y 来表示。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中不需加热的吸热反应是( )
A.锌粒与稀硫酸的反应 B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com