
【题目】几种短周期元素的原子半径及主要化合价如下表
元素代号 | X | Y | Z | M | R | w |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 | 0.077 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 | +4 -4 |
已知:X是短周期中最活泼的金属,且与R同周期。请用相应的化学用语或者化学符号回答下列问题。
(1)R在元素周期表中的位置为________________。
(2)X与M按原子个数比1:1构成的物质的电子式为_____________;所含化学键类型___________。
(3)X+、Y2-、M2-、R3+离子半径大小顺序为__________________________(用离子符号表示)。
(4)请用电子式表示WY2的形成过程___________________________________。
【答案】第三周期IIIA族 ![]() 离子键和共价键 S2->O2->Na+>Al3+
离子键和共价键 S2->O2->Na+>Al3+ ![]()
【解析】
已知X是短周期中最活泼的金属,且与R同周期,则X是Na,R是Al。Y有+6和-2两种价态,则Y是S;M只有-2价,则M是O;Z和W的原子半径相差较小,则根据化合价可知Z是N,W是C。据此解答。
根据以上分析可知X是Na,Y是S,Z是N,M是O,R是Al,W是C。则
(1)Al在元素周期表中的位置为第三周期ⅢA族。
(2)X与M按原子个数比1:1构成的物质是过氧化钠,电子式为![]() ;所含化学键类型为离子键和共价键。
;所含化学键类型为离子键和共价键。
(3)核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则X+、Y2-、M2-、R3+离子半径大小顺序为S2->O2->Na+>Al3+。
(4)CS2是含有极性键的共价化合物,则电子式表示CS2的形成过程为![]() 。
。


科目:高中化学 来源: 题型:
【题目】原子序数为x的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则A、B、C、D四种元素的原子序数之和不可能是(镧系、锕系、0族元素除外)( )
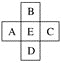
A. 4xB. 4x+14
C. 4x+10D. 4x+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应的生成物Y的浓度在4min内由0变成了4mol/L,则以Y表示该反应在4min内的平均反应速率为 ( )
A. 16 mol/(L·min) B. 4 mol/(L·min)
C. 2 mol/(L·min) D. 1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如下 (图中虚线表示氢键)。下列说法不正确的是( )
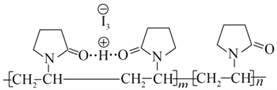
A. 聚维酮的单体是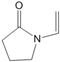 B. 聚维酮分子的聚合度为2m+n
B. 聚维酮分子的聚合度为2m+n
C. 聚维酮在NaOH水溶液中水解可生成 D. 聚维酮和聚维酮碘都是水溶性的
D. 聚维酮和聚维酮碘都是水溶性的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①CH3CH=CHCH3、② ![]() 、③
、③![]() 、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
(1)互为同系物的有___________________(用序号表示)。
(2)互为同位素的有___________________(用序号表示)。
(3)③的系统名称_____________________,②的系统名称_____________________。
(4)写出⑧与Br2 按照1:1发生加成反应所得产物的结构简式______________________________。
(5)等物质的量的⑦和⑩的电子数之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题中信息完成下列填空题
(1)黄绿色气体单质X,与标况下密度为1.25g/L的烯烃Y发生加成反应,请写出烯烃Y的结构式__________。写出该加成产物的所有同分异构体结构简式______________。
(2)125℃,101kPa的条件下,某气态烯烃在氧气中充分燃烧后,气体体积没有变化,求出该烯烃的分子式________。
(3)某元素X的一种核素质量数为A,含N个中子,它与1H原子组成HmX分子。在a g HmX中所含质子的物质的量是___________mol。
(4)E和F均含有18个电子的微粒,E是所有18电子微粒中氧化能力最强的分子,请你写出E与水发生的化学反应方程式_______________。F是有两种元素组成的三原子分子,将其通入足量的NaOH溶液,发生的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在生产生活中有广泛的应用。下列叙述正确的是
A.开发新技术可将水分解成氢气、氧气并释放能量
B.研制新型催化剂可提高汽车尾气的平衡转化率
C.燃料电池能将化学能完全转化为电能
D.为防止金属管道被腐蚀,应将金属管道与电源负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中可以作为2NO2(g) ![]() 2NO(g)+O2(g)达到平衡状态的标志是( )
2NO(g)+O2(g)达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
A. ①③⑤⑦ B. ②④⑤ C. ①③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于将煤转化为水煤气作能源的优点是( )
A.有利于提高燃料的燃烧效率B.有利于减少排放大气污染物
C.有利于管道输送D.有利于放出更多热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com