
【题目】下列关于氯元素的说法正确的是( )
A. HCl具有很强的酸性,且只有氧化性没有还原性
B. ![]() 、
、![]() 为不同的核素,有完全不同的化学性质
为不同的核素,有完全不同的化学性质
C. 1.12L含有1 .7NA个质子(NA表示阿伏加德罗常数)
D. 氯气可从KI溶液中置换出I2,说明氯的非金属性比碘强
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案科目:高中化学 来源: 题型:
【题目】根据部分短周期元素的信息回答问题。
元素 | 元素信息 |
A | 第3周期ⅥA族 |
B | 族序数是周期数的3倍 |
C | 原子序数是11 |
D | D3+与Ne的电子数相同 |
(1)A、B的元素符号为________、________,C、D的元素名称为________、________。
(2)写出B、C的常见单质在加热时的反应方程式:________。
(3)从原子结构的角度分析,A原子与B原子的________相同,C原子与D原子的________相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是重要的漂白剂。某小组开展如下实验,按如图装置制取无水NaClO2晶体,回答下列问题:
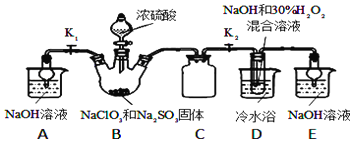
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.
(1)装置C的作用是_________________;
(2)已知装置B中的产物有ClO2气体,则B中反应的方程式为_________________;装置D中反应生成NaClO2的化学方程式为_________________________;
(3)从装置D反应后的溶液中获得无水NaClO2晶体的操作步骤为:①减压,55℃蒸发结晶;②____________;③用38℃~60℃热水________;④在_____________条件下干燥得到成品.
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是_________和____________;
(5)测定样品中NaClO2的纯度.测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+4I-+4H+═2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液.取25.00mL待测溶液,加入淀粉溶液做指示剂,用c molL-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32-═2I-+S4O62-).请计算所称取的样品中NaClO2的物质的量为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都具有10个电子,其结构特点如下:
粒子代码 | a | b | c | d | e | f | g |
原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c和f在一定条件下形成一个g分子和一个d分子,试写出:
(1)a粒子的原子结构示意图___________
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为___>_____ (用化学式表示)。
(3)d与一种含有极性键双核18电子分子反应的化学方程式为 ______。
(4)g与一种含有非极性键双核18电子分子反应的化学方程式为__________
上述反应中,断裂化学键是__________,写出的化学键是________(填“离子键”、“极性键”、“非极性键”、“氢键”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. H2SO4溶于水能电离出H+和SO42-,所以硫酸是离子化合物
B. Ba(OH)2晶体中既存在共价键又有离子键
C. SiO2属于原子晶体,熔化破坏共价键和分子间作用力
D. 干冰升华时,分子内共价键会发生断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据以下数据推断丙烷的沸点可能是( )
物质 | 甲烷 | 乙烷 | 丁烷 | 戊烷 |
沸点 | -162 ℃ | -89 ℃ | -1 ℃ | +36 ℃ |
A. 约-40 ℃ B. 低于-160 ℃
C. 低于-89 ℃ D. 高于+36 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是化学中常用的思维方法。下列推理正确的是
A. Cl2与水反应生成HCl和HClO,推测F2与水反应生成HF和HFO
B. SiH4的沸点高于CH4,推测H2S的沸点高于H2O
C. NH3分子为三角锥型,推测PH3分子三角锥型
D. S与Fe反应生成FeS,推测S与Cu生成CuS
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com