
化学与社会、生活密切相关。下列说法正确的是
A.用钢瓶储存液氯或浓硫酸
B.对石油进行分馏可以得到许多苯的同系物
C.汽车尾气中氮氧化物的产生主要是由于汽油中含有氮元素而产生的
D.在某爆炸事故救援现场,消防员发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:2015-2016学年贵州遵义航天高中高二下期中理综化学试卷(解析版) 题型:选择题
要检验某溴乙烷中的溴元素,正确的实验方法是( )
A.加入氯水振荡,观察水层是否有棕红色出现
B.滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一下期中化学试卷(解析版) 题型:选择题
分子式为C4H10O且可与金属钠反应放出氢气的有机化合物有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:推断题
[化学-选修5:有机化学基础]
可由N物质通过以下路线合成天然橡胶和香料柑青酸甲酯衍生物F

已知:
(1)用系统命名法对N命名 .
(2)①试剂a的名称是________。 ②C D中反应i的反应类型是________。
D中反应i的反应类型是________。
(3)E的结构简式是_____________。
(4)关于试剂b的下列说法不正确是________(填字母序号)。
a. 存在顺反异构体 b. 难溶于水
c. 能发生取代、加成和氧化反应 d. 不能与NaOH溶液发生反应
(5)写出A生成B的反应方程式 。
(6)分子中含有 结构的D的所有同分异构共有________种(含顺反异构体),写出其中任意一种含反式结构的结构简式________。
结构的D的所有同分异构共有________种(含顺反异构体),写出其中任意一种含反式结构的结构简式________。
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是

A.该弱酸在滴定前的浓度大于0.001mol/L
B.由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(Na+) >c(A-) > c(OH-) >c(H+)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:实验题
硫化锌 (ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
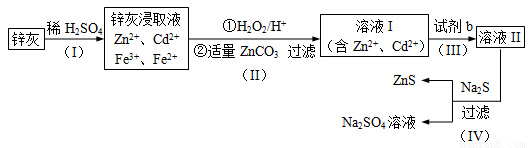
(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为________;
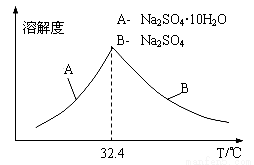
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列事实不能用元素周期律解释的是
A.向Na2SO3溶液中加盐酸,有气泡产生
B.0.1 mol·L-1溶液的pH:NaOH > LiOH
C.Mg、Al与同浓度盐酸反应,Mg更剧烈
D.气态氢化物的稳定性:HBr > HI
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
法国科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性 B.该粒子质量数为4
C.在周期表中与氢元素占同一位置 D.该粒子质量比氢原子大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:填空题
Ⅰ、甲醇是重要的化工原料,在日常生活中有着广泛的应用。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为_________________。
②反应Ⅰ中,若△H1﹤0,则要提高甲醇的产率,可采取的措施有_____(填字母)
A.缩小容器的体积 B.降低温度 C.升高温度
D.使用合理的催化剂 E.将甲醇从混合体系中分离出来
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H1=-1453kJ/mol
②2CO (g)+O2(g)=2CO2(g) △H2=-466kJ/mol
请写出32g甲醇液体发生不完全燃烧生成一氧化碳和液态水的热化学反应方程式: 。
Ⅱ.由CO2和H2合成CH3OH的反应如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H。在10L的恒容密闭容器中投入1 mol CO2和2.75 mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
CH3OH(g)+H2O(g)△H。在10L的恒容密闭容器中投入1 mol CO2和2.75 mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
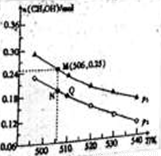
①上述反应的△H (填“﹥”或“﹤”)0
②图中压强p1 (填“﹥”或“﹤”)p2
③经测定知Q点时容器的压强是反应前压强的0.9,若反应从开始到平衡所需的时间为10min,则0~10min内H2的反应速率v(H2)= 。
④N点时,该反应的平衡常数K= (计算结果保留2位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com