
(8分)按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。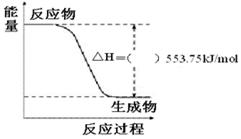
②写出表示丙烷燃烧热的热化学方程式:_______________________________________。
科目:高中化学 来源: 题型:阅读理解
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |

| M | ||
4
|
| M | ||
4
|
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。
②写出表示丙烷燃烧热的热化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年湖北省高二上学期期中考试试题化学 题型:填空题
(8分)按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。

②写出表示丙烷燃烧热的热化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“—”。
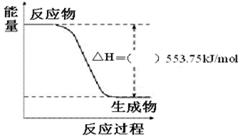
②写出表示丙烷燃烧热的热化学方程式:_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com