

分析 (1)根据反应物的状态和反应条件选择反应装置;
(2)次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的;
(3)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,二氧化硫和氢氧化钠反应生成盐和水;
(4)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应而使气体失去漂白性;
(5)二氧化硫为酸性氧化物,能与碱性氧化物、碱发生反应;二氧化硫能漂白某些有色物质,如使品红溶液褪色;二氧化硫中硫为+4价,属于中间价态,有氧化性又有还原性,以还原性为主,如二氧化硫能使氯水、溴水、KMnO4溶液褪色,体现了二氧化硫的强还原性而不是漂白性.
解答 解:(1)实验室制取氯气所用药品是固体和液体,反应条件是加热,所以应选用固液加热型装置,选E;
故答案为:E;
(2)次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的;加热时,次氯酸漂白过的溶液无变化,二氧化硫和有色物质生成的无色物质不稳定,加热时能重新变成红色;
故答案为:溶液由无色变成红色;
(3)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,二氧化硫和氢氧化钠反应生成盐和水,离子方程式为:SO2+2OH-=SO32-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;SO2+2OH-=SO32-+H2O;
(4)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应而使气体失去漂白性,反应方程式为Cl2+SO2+2H2O=H2SO4+2HCl;
故答案为:Cl2+SO2+2H2O=H2SO4+2HCl;
(5)①二氧化硫使品红溶液褪色体现其漂白性;
②二氧化硫使酸性KMnO4溶液褪色,体现其还原性;
③二氧化硫使溴水褪色,体现其还原性;
④二氧化硫使滴入酚酞的烧碱溶液褪色,是因为二氧化硫为酸性氧化性,与氢氧化钠反应;
⑤二氧化硫使淀粉-碘溶液褪色,体现其还原性;
所以反应实质相同的是②③⑤;
故答案为:D.
点评 本题考查了次氯酸和二氧化硫的漂白性,难度不大,注意次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的,其漂白原理也不同,注意熟悉二氧化硫的性质.


科目:高中化学 来源: 题型:推断题

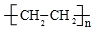 ;⑥
;⑥ +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ +H2O.
+H2O.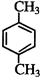 ;
;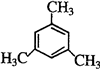 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A. | 反应③最多能产生0.1 mol O2 | |
| B. | 反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ | |
| C. | Na2O2中阴阳离子数目之比为1:1 | |
| D. | ①②③充分反应后所得溶液中溶质的质量分数:②=③>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图小试管中盛有几毫升水,与大试管连通的U形管内放有少量水(已染成红色).如沿小试管壁慢慢注入3mL浓硫酸,静置后,U形管中可观察到的现象是液面( )
如图小试管中盛有几毫升水,与大试管连通的U形管内放有少量水(已染成红色).如沿小试管壁慢慢注入3mL浓硫酸,静置后,U形管中可观察到的现象是液面( )| A. | 左高右低 | B. | 左低右高 | C. | 左右一样高 | D. | 来回振动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原混合气体的体积为1.1VL | |
| B. | 原混合气体的体积为1.2VL | |
| C. | 反应达到限度时,气体A消耗掉0.05 VL | |
| D. | 反应达到限度时,气体B消耗掉0.05 VL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
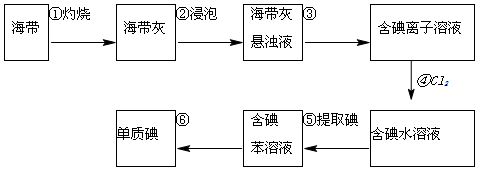 请填写下列空白:
请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾离子受到水分子的作用,克服了离子间的引力,逐渐向水中扩散 | |
| B. | 高锰酸根离子受到钾离子的作用,克服了离子间的斥力,逐渐向水中扩散 | |
| C. | 高锰酸根离子受到水分子的作用,克服了离子间的引力,逐渐向水中扩散 | |
| D. | 高锰酸钾是强氧化剂,水被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+3Y?2Z | |
| C. | 改变温度可以改变此反应的平衡常数 | |
| D. | 增大压强使平衡向生成Z的方向移动,平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 目的 |
| A | 蒸馏 | 分离氯化钠和硝酸钾混合溶液 |
| B | 分液 | 分离乙酸与乙酸乙酯混合物 |
| C | 洗气 | 通入小苏打溶液中除去CO2中的HCl气体 |
| D | 用乙醇作萃取剂 | 提取溴水中的溴单质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com