
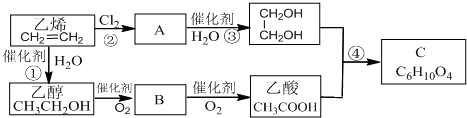
分析 由流程图可知:乙烯与氯气发生加成反应生成物质A,则A为:1,2-二氯乙烷,1,2-二氯乙烷水解生成乙二醇;乙烯与水反应生成乙醇,乙醇发生催化氧化得到物质B,则B为乙醛,乙醛催化氧化得到乙酸;乙酸与乙二醇在浓硫酸条件下发生酯化反应生成二乙酸乙二酯,以此解答该题.
解答 解:乙烯与氯气发生加成反应生成物质A,则A为:1,2-二氯乙烷,1,2-二氯乙烷水解生成乙二醇;乙烯与水反应生成乙醇,乙醇发生催化氧化得到物质B,则B为乙醛,乙醛催化氧化得到乙酸;乙酸与乙二醇在浓硫酸条件下发生酯化反应生成二乙酸乙二酯,
(1)B为乙醛,含有醛基,C为二乙酸乙二酯,含有酯基,故答案为:醛基;酯基;
(2)由以上分析可知A为CH2ClCH2Cl,故答案为:CH2ClCH2Cl;
(3)由合成流程图可知,反应①为乙烯与水的加成反应,反应③为卤代烃的水解生成醇,水解反应为取代反应,故答案为:加成反应;取代反应;
(4)反应②为乙烯与氯气发生加成反应,化学方程式为CH2=CH2+Cl2$→_{△}^{Cu}$CH2ClCH2Cl,
反应④为2CH3COOH+HOCH2-CH2OH$?_{△}^{浓硫酸}$CH3COOCH2-CH2OOCCH3+2 H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;2CH3COOH+HOCH2-CH2OH$?_{△}^{浓硫酸}$CH3COOCH2-CH2OOCCH3+2H2O.
点评 本题考查有机推断题,题目难度中等,涉及官能团名称、物质的结构简式的书写、化学反应的类型判断、化学方程式的书写等知识,熟悉各种物质的结构和性质是解题关键,试题知识点较多,充分考查了学生的分析、理解能力及灵活应用基础知识的能力.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:实验题
 短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学犍 | O=O | C=0 | C≡O |
| 键能(kJ/mol) | 497 | 803 | 1072 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 二氧化碳的晶胞如图,每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为$\frac{\sqrt{2}}{2}$a(其中a为立方体棱长)的CO2有( )
二氧化碳的晶胞如图,每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为$\frac{\sqrt{2}}{2}$a(其中a为立方体棱长)的CO2有( )| A. | 4个 | B. | 8个 | C. | 12个 | D. | 6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液呈电中性,胶体带有电荷 | |
| B. | 溶液中溶质粒子一定不带电,胶体中分散质粒子带有电荷 | |
| C. | 溶液中溶质粒子的运动有规律,而胶体粒子的运动无规律 | |
| D. | 溶液中通过一束光线时无特殊现象,胶体中通过一束光线时有明显的光带 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由分子组成的物质中不一定存在共价键 | |
| B. | 金刚石、石墨、足球烯均是碳元素的同素异形体,性质都相似 | |
| C. | 由非金属元素组成的晶体一定是分子晶体 | |
| D. | 仅由非金属元素组成的物质不可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用盐酸除去铜粉中混有的铁粉 | |
| B. | 用浓盐酸和MnO2制氯气 | |
| C. | 用盐酸跟氢氧化钠溶液反应 | |
| D. | 盐酸和硝酸银溶液反应生成白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com