
вбжЊCO2ЃЈgЃЉЃЋH2ЃЈgЃЉ COЃЈgЃЉЃЋH2OЃЈgЃЉЕФЦНКтГЃЪ§ЫцЮТЖШБфЛЏШчЯТБэЃК
COЃЈgЃЉЃЋH2OЃЈgЃЉЕФЦНКтГЃЪ§ЫцЮТЖШБфЛЏШчЯТБэЃК
| t/Ёц | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
| | A | B | C | D | E |
| nЃЈCO2ЃЉ | 3 | 1 | 0 | 1 | 1 |
| nЃЈH2ЃЉ | 2 | 1 | 0 | 1 | 2 |
| nЃЈCOЃЉ | 1 | 2 | 3 | 0.5 | 3 |
| nЃЈH2OЃЉ | 5 | 2 | 3 | 2 | 1 |
 COЃЈgЃЉЃЋH2OЃЈgЃЉЃЌдкИУШнЦїФкИїЮяжЪЕФХЈЖШБфЛЏШчЯТЃК
COЃЈgЃЉЃЋH2OЃЈgЃЉЃЌдкИУШнЦїФкИїЮяжЪЕФХЈЖШБфЛЏШчЯТЃК| ЪБМф /min | CO2 ЃЈmolЁЄLЃ1ЃЉ | H2 ЃЈmolЁЄLЃ1ЃЉ | CO ЃЈmolЁЄLЃ1ЃЉ | H2O ЃЈmolЁЄLЃ1ЃЉ |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
 ИїЕиЦкФЉИДЯАЬибЕОэЯЕСаД№АИ
ИїЕиЦкФЉИДЯАЬибЕОэЯЕСаД№АИ аЁВЉЪПЦкФЉДГЙи100ЗжЯЕСаД№АИ
аЁВЉЪПЦкФЉДГЙи100ЗжЯЕСаД№АИ УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ
УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
КЯГЩАБФђЫиЙЄвЕЩњВњЙ§ГЬжаЩцМАЕФЮяжЪзЊЛЏЙ§ГЬШчЯТЭМЫљЪОЁЃ
(1)ЬьШЛЦјдкИпЮТЁЂДпЛЏМСзїгУЯТгыЫЎеєЦјЗДгІЩњГЩH2КЭCOЕФЛЏбЇЗНГЬЪНЮЊ___________________________________ЁЃ
(2)дкКЯГЩАБЩњВњжаЃЌНЋЩњГЩЕФАБЦјМАЪБДгЗДгІКѓЕФЦјЬхжаЗжРыГіРДЁЃдЫгУЛЏбЇЦНКтЕФжЊЪЖЗжЮіетбљзіЪЧЗёгаРћгкАБЕФКЯГЩЃЌЫЕУїРэгЩЃК___________ЁЃ
(3)ЯТЭМЮЊКЯГЩАБЗДгІдкВЛЭЌЮТЖШКЭбЙЧПЁЂЪЙгУЯрЭЌДпЛЏМСЬѕМўЯТЃЌГѕЪМЪБЕЊЦјЁЂЧтЦјЕФЬхЛ§БШЮЊ1ЃК3ЪБЃЌЦНКтЛьКЯЮяжаАБЕФЬхЛ§ЗжЪ§ЁЃ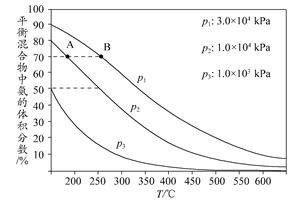
ЂйШєЗжБ№гУvA(NH3)КЭvB(NH3)БэЪОДгЗДгІПЊЪМжСЦНКтзДЬЌAЁЂBЪБЕФЛЏбЇЗДгІЫйТЪЃЌдђvA(NH3)________vB(NH3)(ЬюЁА>ЁБЁЂЁА<ЁБЛђЁАЃНЁБ)ЁЃ
ЂкдкЯрЭЌЮТЖШЯТЃЌЕБбЙЧПгЩp1БфЮЊp3ЪБЃЌКЯГЩАБЗДгІЕФЛЏбЇЦНКтГЃЪ§________(ЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБ)ЁЃ
Ђлдк250ЁуCЁЂ1.0ЁС104kPaЯТЃЌH2ЕФзЊЛЏТЪЮЊ________%(МЦЫуНсЙћБЃСєаЁЪ§ЕуКѓ1ЮЛ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ЕЊМАЦфЛЏКЯЮядкЙЄХЉвЕЩњВњЁЂЩњЛюжагазХживЊзїгУЁЃ
ЃЈ1ЃЉдкTЁцЪБЃЌНЋ0ЃЎ6molH2КЭ0ЃЎ4molN2жУгкШнЛ§ЮЊ2 LЕФУмБеШнЦїжа(бЙЧПЮЊmPa)ЗЂЩњЗДгІЃК3H2+N2 2NH3 ЁїH<0ЁЃШєБЃГжЮТЖШВЛБфЃЌФГаЫШЄаЁзщЭЌбЇВтЕУЗДгІЙ§ГЬжаШнЦїФкбЙЧПЫцЪБМфБфЛЏШчЭМЫљЪОЃК8 minФкЗжжгNH3ЕФЦНОљЩњГЩЫйТЪЮЊ molЁЄL-1ЁЄmin-1ЁЃ
2NH3 ЁїH<0ЁЃШєБЃГжЮТЖШВЛБфЃЌФГаЫШЄаЁзщЭЌбЇВтЕУЗДгІЙ§ГЬжаШнЦїФкбЙЧПЫцЪБМфБфЛЏШчЭМЫљЪОЃК8 minФкЗжжгNH3ЕФЦНОљЩњГЩЫйТЪЮЊ molЁЄL-1ЁЄmin-1ЁЃ
ЃЈ2ЃЉШддкTЁцЪБЃЌНЋ0ЃЎ6molH2КЭ0ЃЎ4molN2жУгквЛШнЛ§ПЩБфЕФУмБеШн ЦїжаЁЃ
ЂйЯТСаИїЯюФмЫЕУїИУЗДгІвбДяЕНЦНКтзДЬЌЕФЪЧ (ЬюађКХ)ЁЃ
aЃЎШнЦїФкN2ЁЂH2ЁЂNH3ЕФХЈЖШжЎБШЮЊlЃК3ЃК2
bЃЎ3vе§(N2)=vФц(H2)
cЃЎ3vе§(H2)=2vФц(NH3)
dЃЎЛьКЯЦјЬхЕФУмЖШБЃГжВЛБф
eЃЎШнЦїжаЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПВЛЫцЪБМфЖјБфЛЏ
ЂкИУЬѕМўЯТДяЕНЦНКтЪБNH3ЕФЬхЛ§ЗжЪ§гыЬтЃЈ1ЃЉЬѕМўЯТNH3ЕФЬхЛ§ЗжЪ§ЯрБШ (ЬюЁАБфДѓЁБЁАБфаЁЁБЛђЁАВЛБфЁБ)ЁЃ
ЂлДяЕНЦНКтКѓЃЌИФБфФГвЛЬѕМўЪЙЗДгІЫйТЪЗЂЩњСЫШчЭМЫљЪОЕФБфЛЏЃЌИФ БфЕФЬѕМўПЩФмЪЧ ЁЃ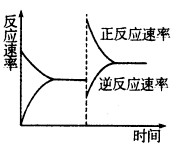
aЃЎЩ§ИпЮТЖШЃЌЭЌЪБМгбЙ
bЃЎНЕЕЭЮТЖШЃЌЭЌЪБМѕбЙ
cЃЎБЃГжЮТЖШЁЂбЙЧПВЛБфЃЌдіДѓЗДгІЮяХЈЖШ
dЃЎБЃГжЮТЖШЁЂбЙЧПВЛБфЃЌМѕаЁЩњГЩЮяХЈЖШ
ЃЈ3ЃЉЯѕЫсГЇЕФЮВЦјКЌгаЕЊбѕЛЏЮяЃЌВЛОДІРэжБНгХХЗХНЋЮлШОПеЦјЁЃ АБЦјФмНЋЕЊбѕЛЏЮяЛЙдЮЊЕЊЦјКЭЫЎЃЌЦфЗДгІЛњРэЮЊЃК
2NH3(g)+5NO2(g)=7NO(g)+3H2O(g)  H=-akJЁЄmol-1
H=-akJЁЄmol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)  H=-bkJЁЄmol-1
H=-bkJЁЄmol-1
дђNH3жБНгНЋNO2ЛЙдЮЊN2ЕФШШЛЏбЇЗНГЬЪНЮЊЃК ЁЃ
ШєБъзМзДПіЯТNOгыNO2ЛьКЯЦјЬх40ЃЎ32LБЛзуСПАБЫЎЭъШЋЮќЪеЃЌВњЩњБъзМзДПіЯТЕЊЦј42ЃЎ56LЁЃИУЛьКЯЦјЬхжаNOгыNO2ЕФЬхЛ§жЎБШЮЊ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ГЌвєЫйЗЩЛњдкЦНСїВуЗЩааЪБЃЌЮВЦјжаЕФNOЛсЦЦЛЕГєбѕВуЁЃПЦбЇМве§дкбаОПРћгУДпЛЏММЪѕНЋЮВЦјжаЕФNOКЭCOзЊБфГЩCO2КЭN2 , ЛЏбЇЗНГЬЪНШчЯТЃК2NO + 2 CO 2CO2 + N2 ЃЌЮЊСЫВтЖЈдкФГжжДпЛЏМСзїгУЯТЕФЗДгІЫйТЪЃЌдкФГЮТЖШЯТЃЌгУЦјЬхДЋИаЦїВтЕУВЛЭЌЪБМфЕФNOКЭCOХЈЖШШчЯТБэЃК
2CO2 + N2 ЃЌЮЊСЫВтЖЈдкФГжжДпЛЏМСзїгУЯТЕФЗДгІЫйТЪЃЌдкФГЮТЖШЯТЃЌгУЦјЬхДЋИаЦїВтЕУВЛЭЌЪБМфЕФNOКЭCOХЈЖШШчЯТБэЃК
| ЪБМф /s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/molЁЄLЁЊ1 | 1.00ЁС10ЁЊ3 | 4.50ЁС10ЁЊ4 | 2.50ЁС10ЁЊ4 | 1.50ЁС10ЁЊ4 | 1.00ЁС10ЁЊ4 | 1.00ЁС10ЁЊ4 |
| c(CO)/molЁЄLЁЊ1 | 3.60ЁС10ЁЊ3 | 3.05ЁС10ЁЊ3 | 2.85ЁС10ЁЊ3 | 2.75ЁС10ЁЊ3 | 2.70ЁС10ЁЊ3 | 2.70ЁС10ЁЊ3 |
| ЪЕбщБрКХ | T / Ёц | NOГѕЪМХЈЖШ ( molЁЄLЁЊ1 ) | COГѕЪМХЈЖШ ( molЁЄLЁЊ1 ) | ДпЛЏМСЕФБШБэУцЛ§ ( m2ЁЄgЁЊ1 ) |
| Ђё | 280 | 1.20 ЁС 10ЁЊ3 | 5.80 ЁС 10ЁЊ3 | 82 |
| Ђђ | | | | 124 |
| Ђѓ | 350 | | | 124 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ЙЄвЕЩЯЩњВњСђЫсЕФСїГЬЭМШчЯТЃК 
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉдчЦкЩњВњСђЫсвдЛЦЬњПѓЮЊдСЯЃЌЕЋЯждкЙЄГЇЩњВњСђЫсвдСђЛЦЮЊдСЯЃЌРэгЩЪЧ ЁЃ
ЃЈ2ЃЉдкЦјЬхНјШыДпЛЏЗДгІЪвЧАашОЛЛЏЕФдвђЪЧ ЁЃ
ЃЈ3ЃЉдкДпЛЏЗДгІЪвжаЭЈГЃЪЙгУГЃбЙЃЌдкДЫЬѕМўЯТSO2ЕФзЊЛЏТЪЮЊ90%ЁЃЕЋЪЧВПЗжЗЂДяЙњМвВЩШЁИпбЙЬѕМўЯТжЦШЁSO3ЃЌВЩШЁМгбЙДыЪЉЕФФПЕФГ§СЫМгПьЗДгІЫйТЪЭтЃЌЛЙПЩвд ЃЌДгЖјЬсИпЩњВњаЇТЪ ЁЃ
ЃЈ4ЃЉЙЄвЕЩњВњжаГЃгУАБЃЫсЗЈНјааЮВЦјЭбСђЃЌвдДяЕНЯћГ§ЮлШОЃЌЗЯЮяРћгУЕФФПЕФЁЃгУЛЏбЇЗНГЬЪНБэЪОЦфЗДгІдРэЃК ЁЃ
ЃЈ5ЃЉГ§СђЫсЙЄвЕЭтЃЌЛЙгааэЖрЙЄвЕЩњВњЁЃЯТСаЯрЙиЕФЙЄвЕЩњВњСїГЬжае§ШЗЕФЪЧ ЁЃ 
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
вЛЖЈЬѕМўЯТЃЌдкЬхЛ§ЮЊ5 LЕФУмБеШнЦїжаЃЌЦјЬЌЮяжЪAЁЂBЁЂCЕФЮяжЪЕФСПn(mol)ЫцЪБМфtЕФБфЛЏШчЭМ1ЫљЪОЁЃвбжЊДяЦНКтКѓЃЌНЕЕЭЮТЖШЃЌAЕФЬхЛ§АйЗжКЌСПНЋМѕаЁЁЃ
(1)ИљОнЩЯЭМЪ§ОнЃЌаДГіЗДгІЕФЛЏбЇЗНГЬЪН ЃЛ
ДгЗДгІПЊЪМЕНЦНКтЪБЕФЦНОљЫйТЪv(C)= ЁЃ
(2)ИУЗДгІЕФІЄH 0(ЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁА=ЁБ)ЁЃ
(3)ДЫЗДгІЦНКтГЃЪ§ЕФБэДяЪНЮЊK= ЁЃ
(4)ИУЗДгІЕФЗДгІЫйТЪvКЭЪБМфtЕФЙиЯЕШчЭМ2ЫљЪОЃК
ЂйИљОнЩЯЭМХаЖЯЃЌдкt3ЪБПЬИФБфЕФЭтНчЬѕМўЪЧ ЁЃ
ЂкAЕФзЊЛЏТЪзюДѓЕФвЛЖЮЪБМфЪЧ ЁЃ
ЂлИїНзЖЮЕФЦНКтГЃЪ§ШчБэЫљЪОЃК
K1ЁЂK2ЁЂK3жЎМфЕФЙиЯЕЮЊЃК (гУЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБСЌНг)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
Н№ЪєУОМАЦфЛЏКЯЮяВЛНідкЙњЗРЩЯгаживЊгІгУЃЌдкЛЏбЇбаОПжавВгаЙуЗКгІгУЁЃ
ЃЈ1ЃЉФГЭЌбЇбаОПЗДгІЫйТЪЪБгУШчЯТЗНЗЈЃКШЁвЛЖЮУОЬѕЃЌгУЩАжНВСШЅБэУцЕФбѕЛЏФЄЃЌЪЙзуСПУОЬѕгывЛЖЈСПбЮЫсЗДгІЩњГЩH2ЕФСПгыЗДгІЪБМфЕФЙиЯЕЧњЯпШчЭМЫљЪОЁЃУОгыбЮЫсЗДгІЕФРызгЗНГЬЪНЮЊ ЃЛдкЧА4minФкЃЌУОЬѕгыбЮЫсЕФЗДгІЫйТЪж№НЅМгПьЃЌдк4 minжЎКѓЃЌЗДгІЫйТЪж№НЅМѕТ§ЃЌЧыМђЪіЦфдвђЃК_____________ЁЃ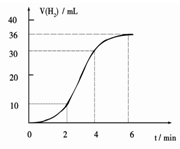
ЃЈ2ЃЉЯђЩйСПЕФMg(OH)2аќзЧвКжаМгШыЪЪСПЕФБЅКЭТШЛЏяЇШмвКЃЌЙЬЬхЭъШЋШмНтЃЌаДГіNH4ClБЅКЭШмвКЪЙMg(OH)2аќзЧвКШмНтЕФРызгЗНГЬЪН ЁЃ
ЃЈ3ЃЉMgЁЁAlПЩаЮГЩдЕчГи:
| БрКХ | ЕчМЋВФСЯ | ЕчНтжЪШмвК | ЕчзгСїЖЏЗНЯђ |
| 1 | MgЁЁAl | ЯЁбЮЫс | MgСїЯђAl |
| 2 | MgЁЁAl | NaOHШмвК | |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ЙЄвЕжЦСђЫсЕФЙ§ГЬжаРћгУЗДгІ2SO2ЃЈgЃЉЃЋO2ЃЈgЃЉ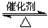 2SO3ЃЈgЃЉЃЛЁїHЃМ0ЃЌНЋSO2зЊЛЏЮЊSO3ЃЌЮВЦјSO2ПЩгУNaOHШмвКНјааЮќЪеЁЃЧыЛиД№ЯТСаЮЪЬтЃК
2SO3ЃЈgЃЉЃЛЁїHЃМ0ЃЌНЋSO2зЊЛЏЮЊSO3ЃЌЮВЦјSO2ПЩгУNaOHШмвКНјааЮќЪеЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉвЛЖЈЬѕМўЯТЃЌЯђвЛДјЛюШћЕФУмБеШнЦїжаГфШы2molSO2КЭ1molO2ЗЂЩњЗДгІЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ ЁЃ
AЃЎШєЗДгІЫйТЪv(SO2)=v(SO3)ЃЌдђПЩвдЫЕУїИУПЩФцЗДгІвбДяЕНЦНКтзДЬЌ
BЃЎБЃГжЮТЖШКЭШнЦїЬхЛ§ВЛБфЃЌГфШы2 mol N2ЃЌЛЏбЇЗДгІЫйТЪМгПь
CЃЎЦНКтКѓНідіДѓЗДгІЮяХЈЖШЃЌдђЦНКтвЛЖЈгввЦЃЌИїЗДгІЮяЕФзЊЛЏТЪвЛЖЈЖМдіДѓ
DЃЎЦНКтКѓвЦЖЏЛюШћбЙЫѕЦјЬхЃЌЦНКтЪБSO2ЁЂO2ЕФАйЗжКЌСПМѕаЁЃЌSO3ЕФАйЗжКЌСПдіДѓ
EЃЎБЃГжЮТЖШКЭШнЦїЬхЛ§ВЛБфЃЌЦНКтКѓдйГфШы2molSO3ЃЌдйДЮЦНКтЪБИїзщЗжХЈЖШОљБШдЦНКтЪБЕФХЈЖШДѓ
FЃЎЦНКтКѓЩ§ИпЮТЖШЃЌЦНКтГЃЪ§KдіДѓ
ЃЈ2ЃЉНЋвЛЖЈСПЕФSO2ЃЈgЃЉКЭO2ЃЈgЃЉЗжБ№ЭЈШыЕНЬхЛ§ЮЊ2LЕФКуШнУмБеШнЦїжаЃЌдкВЛЭЌЮТЖШЯТНјааЗДгІЕУЕНШчЯТБэжаЕФСНзщЪ§ОнЃК
| ЪЕбщБрКХ | ЮТЖШ/Ёц | Ц№ЪМСП/mol | ЦНКтСП/mol | ДяЕНЦНКтЫљашЪБМф/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0ЃЎ8 | 6 |
| 2 | T2 | 4 | 2 | 0ЃЎ4 | y | 9 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ЙЄвЕЩЯжЦШЁШ§бѕЛЏСђЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊЃК
2SO2(g)ЪЎO2(g)  2SO3(g) ЁїH=Ѓ198kJЁЄmol-1
2SO3(g) ЁїH=Ѓ198kJЁЄmol-1
ЃЈ1ЃЉФмЙЛЫЕУїдкКуЮТКуШнЬѕМўЯТЃЌЩЯЪіЗДгІвбОДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ (ЬюађКХ)ЁЃ
AЃЎУПЩњГЩ1mol SO3ЕФЭЌЪБЩњГЩ0ЃЎ5mol O2
BЃЎШнЦїжаЛьКЯЦјЬхЕФУмЖШВЛБф
CЃЎSO2ЁЂO2ЁЂSO3ЕФЮяжЪЕФСПжЎБШЮЊ2ЃК1ЃК2
DЃЎШнЦїжаЦјЬхзмбЙЧПВЛБф
ЃЈ2ЃЉ400ЁцЃЌ1ЃЎ01ЁС105PaЯТЃЌЩЯЪіЗДгІжаn(SO3)КЭn(O2)ЫцЪБМфБфЛЏЕФЙиЯЕШчЭМЫљЪОЁЃЯТСаа№Ъіе§ШЗЕФЪЧ (ЬюађКХ)ЁЃ
AЃЎЕуaЕФе§ЗДгІЫйТЪБШЕуbЕФДѓ
BЃЎЕуcДІЗДгІДяЕНЦНКтзДЬЌ
CЃЎЕуdКЭЕуeДІЕФn(O2)ЯрЭЌ
DЃЎ500ЁцЃЌ1ЃЎ01ЁС105PaЯТЃЌЗДгІДяЕНЦНКтЪБЃЌn(SO3)БШЭМжаeЕуЕФжЕДѓ
ЃЈ3ЃЉвбжЊИУЗДгІЕФK(400Ёц)=7200mol-1ЁЄLЁЃдк400ЁцЪБЃЌШнЛ§ЮЊ1ЃЎ0LЕФУмБеШнЦїжаГфШы0ЃЎ05mol SO2(g)КЭ0ЃЎ03mol O2(g)ЃЌЗДгІвЛЖЮЪБМфКѓЃЌга0ЃЎ04mol SO3ЩњГЩЁЃДЫЪБЃЌИУЗДгІ (ЬюЁАЪЧЁБЁЂЁАЗёЁБЛђЁАЮоЗЈХаЖЯЁБ)ДяЕНЛЏбЇЦНКтзДЬЌЃЌРэгЩЪЧ ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com