

| x |
| 7-x+11-.05x+x+82 |
| 1400 |
| 207 |
| ||
| 7 |


 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| Br2/CCl4 |
| NaOH/H2O |
| O2Cu |
| O2/���� |
| һ������ |
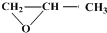 �������Ʒ�Ӧ�ٵķ�Ӧ����д������һ�ֲ���Ľṹ��ʽ
�������Ʒ�Ӧ�ٵķ�Ӧ����д������һ�ֲ���Ľṹ��ʽ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
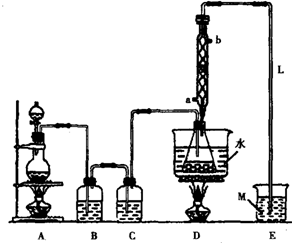
| �� |
| ���� ���� | �۵� | �е� | �Ż�� | �������� |
| ��� | 119.2�� | 446.6�� | 363�� | / |
| ��� | 112.8�� | 446.6�� | 363�� | / |
| S2Cl2 | -77�� | 137�� | / | ��ˮǿ�ҷֽ�����S��SO2��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������������Ż�Ӧ���ȹص���բ |
| B������ʵ�������д����Ŀ�ȼ������й©ʱ��Ӧ��������ͨ�� |
| C��������ϡ���ὦ���۾��Ӧ�����ô���ˮ��ϴ����ϴ��գ�۾� |
| D������������Ũ���Ƥ���ϣ�Ӧ������ˮ��ϴ��Ȼ��Ϳ��3%��ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
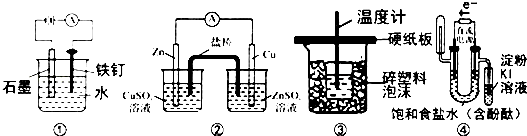
| A���ٷ�ֹ�������� |
| B���ڹ���ͭпԭ��� |
| C�����к��Ȳⶨ |
| D������֤NaCl��Һ������̪�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaCl��Na2CO3�����ܽ⣬�����������ᣬ�����ᾧ |
| B��Na2SO4��NH4Cl�������ȡ����� |
| C��CO2��CO����ͨ������CuO��ĩ |
| D��H2��NH3����ͨ��ʢŨH2SO4��ϴ��ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��������ϩ�ķ���ʽΪC22H26O2 |
| B��������ϩ����FeCl3��Һ������ɫ��Ӧ |
| C��������ϩ�ܷ�����������ԭ����ȥ��ˮ��ȷ�Ӧ |
| D��lmol������ϩ�������5 mol���������ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͨ��HCl���� |
| B�����백ˮ |
| C�������Ҵ� |
| D����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com