
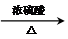 CH3COOCH2-CH2OOCCH3+2H2O.
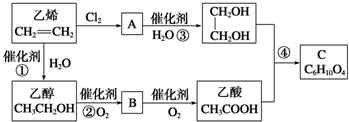
CH3COOCH2-CH2OOCCH3+2H2O.分析 乙烯和氯气发生加成反应生成A,A为CH2ClCH2Cl,A发生水解反应生成HOCH2CH2OH,乙烯和水发生加成反应生成乙醇,乙醇发生催化氧化反应生成B,B为CH3CHO,B发生氧化反应生成CH3COOH,HOCH2CH2OH和CH3COOH发生酯化反应生成C,根据C分子式知,C结构简式为CH3COOCH2CH2OOCCH3,以此解答该题.
解答 解:乙烯和氯气发生加成反应生成A,A为CH2ClCH2Cl,A发生水解反应生成HOCH2CH2OH,乙烯和水发生加成反应生成乙醇,乙醇发生催化氧化反应生成B,B为CH3CHO,B发生氧化反应生成CH3COOH,HOCH2CH2OH和CH3COOH发生酯化反应生成C,根据C分子式知,C结构简式为CH3COOCH2CH2OOCCH3,
(1)由以上分析可知A为ClCH2CH2Cl,故答案为:ClCH2CH2Cl;
(2)C结构简式为CH3COOCH2CH2OOCCH3,C中官能团名称为酯基,故答案为:酯基;
(3)①的反应类型为 加成反应,故答案为:加成;
(4))④为乙二醇与乙酸在浓硫酸条件下发生酯化反应,化学方程式为:HOCH2CH2OH+2CH3COOH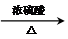 CH3COOCH2CH2OOCCH+2H2O,
CH3COOCH2CH2OOCCH+2H2O,
故答案为:2CH3COOH+HOCH2-CH2OH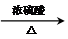 CH3COOCH2-CH2OOCCH3+2H2O;
CH3COOCH2-CH2OOCCH3+2H2O;
(5)B为乙醛,含有醛基,可与氢氧化铜发生氧化还原反应,反应的方程式为CH3CHO+2Cu(OH)2+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$CH3COONa+Cu2O↓+3H2O,
故答案为:CH3CHO+2Cu(OH)2+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$CH3COONa+Cu2O↓+3H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确官能团及其性质关系是解本题关键,熟练掌握常见有机反应类型、有机物官能团及其性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
 ,其阴阳离子个数比为1:2.
,其阴阳离子个数比为1:2.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
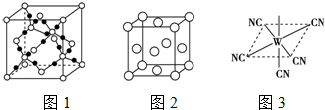
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原产物为NH4+ | |
| B. | 若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ | |
| C. | Fe3+和Fe2+分别属于反应物和生成物 | |
| D. | 氧化剂与还原剂的物质的量之比为1:8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与过量稀硝酸反应:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O | |
| B. | 将铜与硫单质混合加热:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| C. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
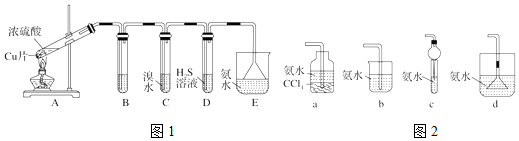
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com