
���෨�ڻ�ѧ�ķ�չ���dz���Ҫ�����ã����з������������( )
�� ����һ��������������ԭ�ӵ���Ŀ������ֳ�һԪ�ᡢ��Ԫ��ȣ�
�� ���ݷ�Ӧ���Ƿ��е���ת�ƽ���ѧ��Ӧ��Ϊ������ԭ��Ӧ�ͷ�������ԭ��Ӧ��
�� ���ݷ�ɢϵ�Ƿ���ж��������ɢϵ��Ϊ��Һ���������Һ��
�� �����Ƿ���ͬ��Ԫ����ɽ����ʷ�Ϊ������ͻ���
�� ������ˮ��Һ�Ƿ��ܹ����罫�������Ϊ����ʺͷǵ���ʡ�
A. �ڢ� B. �٢ڢ� C. �٢� D. ֻ�Т�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�������и�����ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
�������Ǵӻƻ�������ȡ��һ����ɫ��״���壬˫���������������ص���Ҫ�������ű����Ч���������أ���ش��������⣺
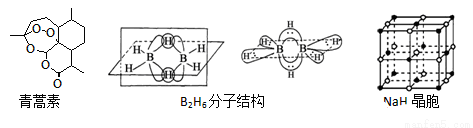
(1)��������ص�����Ԫ�ص縺���ɴ�С������__________��������̬Oԭ�ӵļ۵����Ų�ͼ__________��
(2)һ�������ط����к���_______������̼ԭ�ӡ�
(3)˫�������صĺϳ�һ���������⻯��(NaBH4)��ԭ�����أ����⻯��ĺϳɷ����У�
2LiH+B2H6=2LiBH4�� 4NaH+BF3�TNaBH4+3NaF
��д��BH4���ĵȵ�����_________�����ӡ����Ӹ�дһ�֣���
��B2H6���ӽṹ��ͼ��2��Bԭ�Ӻ�һ��Hԭ�ӹ���2�������γ�3���Ķ����Ӽ����м��2����ԭ�ӱ���Ϊ������ԭ�ӡ�������������2��Bԭ�ӣ���B2H6��������______�ֹ��ۼ���Bԭ�ӵ��ӻ���ʽΪ________ ��
��NaBH4����������һ��Bԭ�����γ�4�����ۼ���������ʯ(Na3AlF6)����������һ��Alԭ�ӿ����γ�6�����ۼ���ԭ����______________��
��NaH�ľ�����ͼ����NaH�����������ӵ���λ����_________���辧��������������Ϊ����������ǡ�����У������������ӵİ뾶��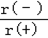 =__________��
=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��ɳ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л���Ľṹ��ʽΪ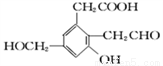 ��ȡNa��NaOH��H2�ֱ�������ʵ����ĸ�����ǡ�÷�Ӧ����Ӧʱ�ɼ�����У�����Na��NaOH��H2�������ʵ����ʵ���֮��Ϊ
��ȡNa��NaOH��H2�ֱ�������ʵ����ĸ�����ǡ�÷�Ӧ����Ӧʱ�ɼ�����У�����Na��NaOH��H2�������ʵ����ʵ���֮��Ϊ
A. 3��2��5 B. 3��3��4 C. 3��2��4 D. 1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㶫ʡ2016-2017ѧ���һ��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
���ʵķ�����ж��ַ��������ж��������������ͼ��
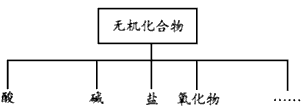
��1����ͼ��ʾ�����ʷ����������____________________��
��2����K��Na��H��O��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±��Тڡ��ܡ����档
������� | �� | �� | �� | ������ | �⻯�� |
��ѧʽ | ��HNO3 ��_______ | ��NaOH ��_______ | ��Na2SO4 ��_______ | ��CO2 ��SO3 | ��NH3 |
��3��д�����������Ģ���Һ��Ӧ�����ӷ���ʽ_______________________��
��4��д���������Һ��Ӧ�Ļ�ѧ����ʽ______________________��
��5����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL 1 mol�� L��1��ϡ���ᡣ
�ɹ�ѡ�õ������У��ٽ�ͷ�ιܢ���ƿ���ձ��� ��������ҩ�ע���Ͳ��������ƽ��

��ش��������⣺
a������������ʵ���Ũ��Ϊ __________ mol�� L��1��
b������ϡ����ʱ����ȱ�ٵ������� ______________ (д��������)��
c�������㣬����480mL 1mol�� L��1��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ_________mL��
d���������Ƶ�ϡ������вⶨ��������Ũ�ȴ���1 mol�� L��1�����ƹ��������и�������������������ԭ���� ___________��
A������ʱ����������ƿ�̶��߽��ж��� ��
B����ϡ�ͺ��ϡ��������ת������ƿ�����žͽ����Ժ��ʵ�������
C��ת����Һʱ��������������Һ��������ƿ���档
D������ƿ������ˮϴ�Ӻ�δ���������������ˮ ��
E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㶫ʡ2016-2017ѧ���һ��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����( )
A. ��FeCl3��Һ��ʴͭ��·�壺Cu + Fe3+ �� Cu2+ + Fe2+
B. Na2O2������H2O��Ӧ����O2 ��2Na2O2 + 2H2O �� 4Na+ + 4OH�� + O2��
C. Ba(OH)2��Һ�м���ϡ���� Ba2+ + OH�� + H+ + SO42-�� BaSO4��+ H2O
D. ���Ȼ�����Һ�м�������İ�ˮ��Al3+ + 4NH3��H2O = AlO2- + 4NH4+ + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ̨���и�һ��ѧ����ĩ�����������Ի�ѧ�Ծ��������棩 ���ͣ������
����һƿ��ɫ�������Һ�����������������еļ�����ɣ�Na+��K+��NH4+��Fe2+��SO42����I����CO32����Cl����SO32����MnO4�������������ʵ�鲽�輰����ش����⣺
����һ��ȡ��������Һ������NaOH��Һ�����ȣ��õ���ҺA���������̼�����ζ������
�����������ҺA��������ϡ�����BaCl2��Һ���õ���ҺB����ɫ�������д̼�����ζ������
����������B��Һ��ͨ������Cl2���õ��ƺ�ɫ��ҺC
��1�������йظ���Һ˵����ȷ����__________��
A. һ������SO42����I����NH4+��SO32��
B. һ��������Fe2+��CO32����MnO4��
C. ���ܴ���CO32����Cl����Na+��K+
D. ����AgNO3��Һȷ��ԭ��Һ���Ƿ����Cl��
��2���������õ��ƺ�ɫ��Һ�����ӷ���ʽ��____________��
��3������ԭ��Һ���ȼ������������ᣬ�ټ���������________���ѧʽ�������ȣ�ͨ������Ҳ�ܵó�����һ������ͬ�Ľ��ۡ�
��4��������Һ�л����ܴ��ڵ������ӣ�ȷ������ڵ�ʵ�鷽����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ̨���и�һ��ѧ����ĩ�����������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ�еĵ���ȡ������ʵ���У�����˵������ȷ����
A. ��Һ©��ʹ��ǰҪ�������Ƿ�©ˮ
B. ��ȡ��Ҫ������ˮ���ұ�ˮ������ʹ���ܽ�
C. ��CCl4����ȡ������ȡ��Һ��ֲ����²���ɫ
D. ��Һʱ����������ʹ�²�Һ���������ϲ�Һ����Ͽڵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ̨���и�һ��ѧ����ĩ�����������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
2Mg+CO2 2MgO+C�ķ�Ӧ��������
2MgO+C�ķ�Ӧ��������
A. ���ֽⷴӦ B. �û���Ӧ C. ���Ϸ�Ӧ D. �ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��һ��ѧ�ڵ�һ��ģ�鿼�Ի�ѧ�Ծ��������棩 ���ͣ�������
�����£���20.0 g��������Ϊ14.0%��KNO3��Һ��30.0 g��������Ϊ24.0%��KNO3��Һ��ϣ��õ����ܶ�Ϊ1.15 g/cm3�Ļ����Һ�����㣺
��1����Ϻ���Һ������������
��2����Ϻ���Һ�����ʵ���Ũ�ȡ�
��3����1 000 gˮ�����ܽ����Ħ��KNO3����ʹ��Ũ��ǡ����������Ϻ���Һ��Ũ����ȣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com