
| A. | 构成原电池正极和负极的材料必须是两种金属 | |
| B. | 由铜、锌电极与硫酸铜溶液组成的原电池中铜是负极 | |
| C. | 电子由锌片流经稀硫酸溶液到铜片,氢离子在铜片上得到电子放出氢气 | |
| D. | 铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过 |
分析 A、构成原电池正极和负极的材料只要是活泼性不同即可;
B、由铜、锌电极与硫酸铜溶液组成的原电池中,失电子的是锌;
C、由铜、锌电极与硫酸铜溶液组成的原电池中,氢离子在铜片上得到电子放出氢气;
D、铜锌原电池工作时,负极上发生反应Zn-2e-=Zn2+,据此计算.
解答 解:A、构成原电池正极和负极的材料不一定是两种金属,也可以是一种金属和一种非金属,故A错误;
B、由铜、锌电极与硫酸铜溶液组成的原电池中失电子的是锌,所以锌是负极,故B错误;
C、电子由锌片流经导线而不是经稀硫酸溶液到铜片,氢离子在铜片上得到电子放出氢气,故C错误;
D、铜锌原电池工作时,负极上发生反应Zn-2e-=Zn2+,若有13g锌即0.2mol锌被溶解,电路中就有0.4mol电子通过,故D正确;
故选D.
点评 本题涉及原电池正负极的选择和判断,原电池的简单计算等知识,属于综合中知识的考查,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 可加入硫酸以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 充电过程中,电池正极材料的质量增加 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| D | ||
| A | B | C |
| E |
| A. | 5Z | B. | 5Z+8 | C. | 5Z+10 | D. | 5Z+18 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期p区元素,有种单质常作电极材料 | 基态原子2p能级上各轨道中均有电子且电子的自旋方向相同 | 基态原子的核外电子共有17种运动状态 | 位于第四周期第VA族 |
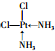 (YH3作为一个整体写)
(YH3作为一个整体写)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti原子中均含有22个中子 | |
| B. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti质子数相同 | |
| C. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti质量数不同,不能互称同位素 | |
| D. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti化学性质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.010mol/(L•s) | B. | v(O2)=0.10mo1/(L•s) | ||
| C. | v(NO)=0.10mo1/(L•s) | D. | v(H2O)=0.30mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
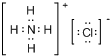 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D是由短周期元素形成的单质.B、E均为组成空气的成分.化合物F的焰色反应呈黄色.在G中,非金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
A、B、C、D是由短周期元素形成的单质.B、E均为组成空气的成分.化合物F的焰色反应呈黄色.在G中,非金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出): .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com