

 FeO+CO↑+CO2↑(2分)
FeO+CO↑+CO2↑(2分) Fe(OH)3+3H+(2分) ; 5(2分) (4)6Fe2O3
Fe(OH)3+3H+(2分) ; 5(2分) (4)6Fe2O3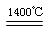 4Fe3O4+O2↑(2分);
4Fe3O4+O2↑(2分); FeC2O4·(2-n)H2O+nH2O
FeC2O4·(2-n)H2O+nH2O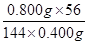 =
=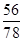 ,因此该化合物是氧化亚铁,其化学式是FeO,所以反应的化学方程式是FeC2O4
,因此该化合物是氧化亚铁,其化学式是FeO,所以反应的化学方程式是FeC2O4 FeO+CO↑+CO2↑。
FeO+CO↑+CO2↑。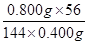 =0.70,因此该固体是氧化铁。氧化铁溶于盐酸生成氯化铁,铁离子水解溶液显酸性,其离子方程式是Fe3++3OH-
=0.70,因此该固体是氧化铁。氧化铁溶于盐酸生成氯化铁,铁离子水解溶液显酸性,其离子方程式是Fe3++3OH- Fe(OH)3+3H+。根据氢氧化铁的溶度积常数可知,当溶液中铁离子的离子浓度为4.0x10-11mol/L时,溶液中c(OH-)=
Fe(OH)3+3H+。根据氢氧化铁的溶度积常数可知,当溶液中铁离子的离子浓度为4.0x10-11mol/L时,溶液中c(OH-)=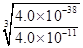 =10-9mol/L,所以溶液中c(H+)=10-5mol/L,因此pH=5。
=10-9mol/L,所以溶液中c(H+)=10-5mol/L,因此pH=5。 4Fe3O4+O2↑;产生特征蓝色沉淀的离子反应方程式3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓或K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓。
4Fe3O4+O2↑;产生特征蓝色沉淀的离子反应方程式3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓或K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓。

科目:高中化学 来源:不详 题型:实验题
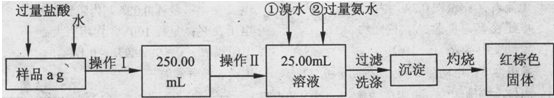
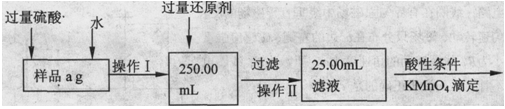
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2FeCl2+CuCl2。现向FeCl3溶液中加入a g Cu粉,完全溶解后,再加入b g Fe粉,充分反应后尚有c g残余固体。若c<a,则下列说法正确的是
2FeCl2+CuCl2。现向FeCl3溶液中加入a g Cu粉,完全溶解后,再加入b g Fe粉,充分反应后尚有c g残余固体。若c<a,则下列说法正确的是| A.残余固体全部是Cu |
| B.残余固体可能为Fe和Cu的混合物 |
| C.最后得到的溶液可能含有Fe3+ |
| D.残余固体是Fe,溶液中一定不含Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
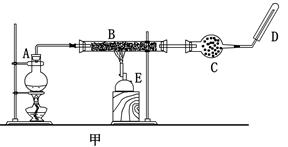
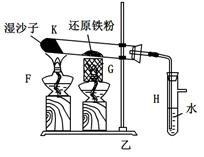
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①② | B.②⑨ | C.⑨④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
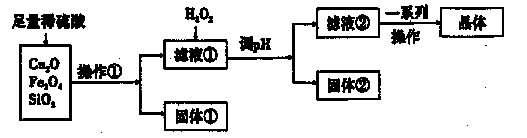
| A.NaOH溶液 | B.CuO | C.氨水 | D.CuCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属与盐溶液间的反应一定是置换反应 |
| B.能与酸反应的氧化物一定是碱性氧化物 |
| C.1 1H2和2 1H2的物理性质略有差异,化学性质几乎完全相同 |
| D.常见金属铁和铝在工业上是由热还原法制得的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com