
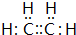 ;C的分子式是C2H4O.
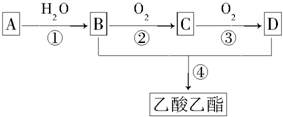
;C的分子式是C2H4O.分析 B连续发生氧化反应生成D,二者反应得到乙酸乙酯,则B为CH3CH2OH,D为CH3COOH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应生成乙酸,A是气态烃,与水反应生成乙醇,A和甲是“来自石油和煤的两种基本化工原料”,则A为CH2=CH2,甲为苯,以此解答该题.
解答 解:B连续发生氧化反应生成D,二者反应得到乙酸乙酯,则B为CH3CH2OH,D为CH3COOH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应生成乙酸,A是气态烃,与水反应生成乙醇,A和甲是“来自石油和煤的两种基本化工原料”,则A为CH2=CH2,甲为苯,
(1)由上述分析可知,A为CH2=CH2,电子式为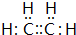 ,C为乙醛,分子式为C2H4O,故答案为:
,C为乙醛,分子式为C2H4O,故答案为: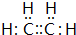 ;C2H4O;
;C2H4O;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛,反应③是乙醛发生氧化反应生成乙酸,反应④是乙酸与乙醇发生酯化反应生成乙酸乙酯,也属于取代反应,故答案为:①;
(3)反应④的化学反应方程式:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,B→C是乙醇氧化生成乙醛,反应方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(4)由于乙酸具有酸性,乙醇溶于水,而苯与水溶液不互溶,可以碳酸钠溶液鉴别B(乙醇)、D(乙酸)和甲(苯),故答案为:饱和Na2CO3溶液.
点评 本题考查有机物的推断,为高频考点,侧重学生的分析能力的考查,涉及烯烃、醇、醛、羧酸的性质与转化,题目难度不大,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:解答题
 某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验).
某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验).| 实验操作 | 实验现象 | |
| I | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色. |
| II | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化. |
| III | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56 | B. | 157 | C. | 258 | D. | 101 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
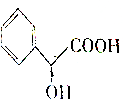 下列说法正确的是( )
下列说法正确的是( )| A. | 扁桃酸分子至多有10个原子在同一平面 | |
| B. | 扁桃酸在一定条件下能发生消去反应 | |
| C. | 某酯与扁桃酸互为同分异构体,苯环上有2个取代基且能与氯化铁发生显色反应,该酯的结构有3种 | |
| D. | 由苯乙烯(C6H5CH=CH2)合成扁桃酸需经过加成→水解→氧化→还原等步骤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
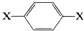 ,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )
,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )| A. | 该有机物燃烧时一定只生成CO2和H2O | |
| B. | 该有机物不可能为芳香醇 | |
| C. | 该有机物的分子式可能为C8H10O2 | |
| D. | 该有机物可能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
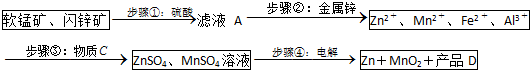
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com