
下列说法正确的是( )
A、燃料电池由外设装备提供燃料和氧化剂
B、Mg和Al通常用热还原的方法来冶炼
C、绿色化学的核心是应用化学原理对环境污染进行治理
D、蛋白质、棉花、淀粉、油脂都是由高分子组成的物质
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
工业上冶炼金属钼的化学原理为:
①2MoS2+7O2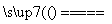 2MoO3+4SO2;
2MoO3+4SO2;
②MoO3+2NH3·H2O = (NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl = H2MoO4↓+2NH4Cl;
④H2MoO4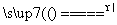 MoO3+H2O;
MoO3+H2O;
⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是
A.上述①③⑤属于氧化还原反应,②④属于非氧化还原反应
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和Al分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D均为中学常见物质, 其中A为单质,B、C、D为化合物,并且存在如下转化关系:试回答下列问题:
其中A为单质,B、C、D为化合物,并且存在如下转化关系:试回答下列问题:
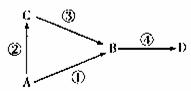
(1)若A为空气的主要成分,B与D为氧化物,试写出D对大气的一种危害 ;
(2)若A为淡黄色非金属单质,B为气态氧化物,是空气的重要污染物之一,C为气态氢化物。试写出B与C反应的化学方程式____
(3)若A为金属单质,且D为红褐色不溶性固体,则反应③的离子方程式为_ 。
(4)B与C为氧化物,D是一种盐,俗名纯碱
①若A为金属单质,写出反应④的化学方程式为 ;
②若A为非金属单质,则符合转化④的一个反应的离子方程式为 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:
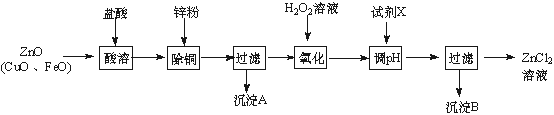
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为
1.0 mol·L-1计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1. 1 | 3. 2 |
| Zn2+ | 5. 2 | 6. 4 |
| Fe2+ | 5. 8 | 8. 8 |
(1)加入H2O2溶液发生反应的离子方程式为 ▲ 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 ▲ (选填序号:a.ZnO;b.Zn(OH)2 ; c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 ▲ 。
(3)氯化锌能催化乳酸(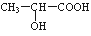 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ▲ ;阴极的电极反应为 ▲ 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将分别含有甲、乙两种常见金属元素的两种正盐A和B的混合物溶于水,通入氯气,然后向反应后的溶液中加入四氯化碳并振荡、静置,溶液分层,下层液体呈橙红色。若在该混合物的溶液中滴加一定浓度的氨水至过量,可得到白色沉淀C。向沉淀C加入过量NaOH溶液,沉淀部分溶解,剩余白色沉淀D。将D溶于盐酸,可得到A溶液;将D灼烧可得到优质的耐高温材料。
(1)试写出A和B的化学式:A ,B 。
(2)元素乙的单质可与某黑色固体反应置换出熔融态的铁,写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为短周期的一部分,Y原子最外层电子数
是其电子层数的2倍,下列说法正确的是( )

A.Y的氢化物比Z的氢化物稳定
B.原子半径大小顺序是X >Y>R
C.Y、R形成的化台物YR2能使酸性KMnO4溶液褪色
D.四种元素中最高价氧化物的水化物的酸性最强的是Y
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族。下列推断不正确的是 ( )
A、A、B、E一定在不同周期 B、C的最高价氧化物的水化物可能显碱性
C、A、D可能在同一主族 D、C和D的单质可能化合形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
用括号中注明的方法分离下列各组混合物,其中不正确的是 ( )
A.氮气和氧气(液化蒸馏)
B.食盐中的沙砾(溶解过滤)
C.氢氧化铁胶体中的少量食盐(渗析)
D.除去乙醇中溶解的微量食盐(过滤)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com