
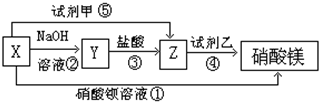
分析 X与硝酸钡反应得到硝酸镁,则X含有镁离子,且阴离子与钡离子反应生成沉淀,可推知X为MgSO4,结合转化关系,可知Y为Mg(OH)2、Z为MgCl2、试剂甲为 BaCl2,试剂乙为AgNO3,据此解答.
解答 解:(1)X与硝酸钡反应得到硝酸镁,则X含有镁离子,且阴离子与钡离子反应生成沉淀,可推知X为MgSO4,结合转化关系,可知Y为Mg(OH)2、Z为MgCl2、试剂甲为 BaCl2,试剂乙为AgNO3,
故答案为:MgSO4;Mg(OH)2; MgCl2;BaCl2;AgNO3;
(2)反应①的离子方程式为:SO42-+Ba2+═Ba(SO4)2↓;
反应②的离子方程式为:Mg2++2OH-═Mg(OH)2↓;
反应③的离子方程式为:Mg(OH)2+2H+═Mg2++2H2O;
反应④的离子方程式为:Ag++Cl-═AgCl↓,
故答案为:SO42-+Ba2+═Ba(SO4)2↓;Mg2++2OH-═Mg(OH)2↓;Mg(OH)2+2H+═Mg2++2H2O;Ag++Cl-═AgCl↓.
点评 本题考查无机物推断,充分利用X与硝酸钡发生的复分解反应进行推断,有利于基础知识的巩固.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色、纯净的Fe(OH)2沉淀,应用如图所示电解实验可制得白色、纯净的Fe(OH)2沉淀,两电极的材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色、纯净的Fe(OH)2沉淀,应用如图所示电解实验可制得白色、纯净的Fe(OH)2沉淀,两电极的材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在室内种植芦荟、常青藤等绿色植物 | |
| B. | 随意对室内装饰 | |
| C. | 不要紧闭门窗,注意经常保持通风 | |
| D. | 室内有异味时,要即时多喷洒香水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com